4 月 3 日,CDE 官网显示,海和药物申报的艾普美妥司他片上市申请获得受理,拟用于治疗不可手术的局部晚期或转移性经治上皮样肉瘤(ES)患者,此前该适应症已被纳入优先审评。
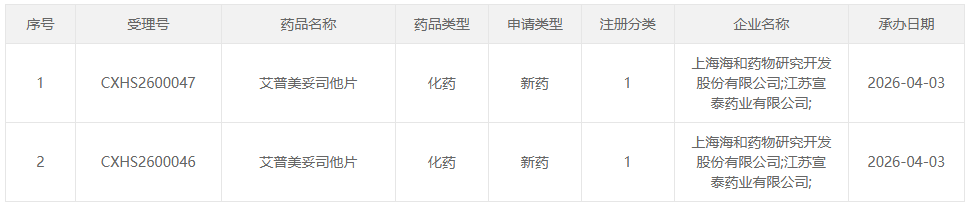
截图来源:CDE 官网
艾普美妥司他(研发代号:HH2853)是一款强效、高选择性的 EZH1/2 小分子抑制剂,抑制 EZH2 的同时也有效抑制 EZH1 的补偿作用。
临床前研究表明,艾普美妥司他能强效抑制细胞内的整体 H3K27me3 水平,在外周 T 细胞性淋巴瘤(PTCL)、含有 EZH2 突变的弥漫性大 B 细胞淋巴瘤(DLBCL)以及含有 SWI/SNF 复合物亚基突变的多种实体瘤模型中,艾普美妥司他 均显示强效的体内外抗肿瘤活性,且在同等剂量下,艾普美妥司他抗肿瘤活性与他泽司他相比更优。
ES 是一种罕见的侵袭性软组织肉瘤,占所有软组织肉瘤比例不足 1%,其远端型好发于青壮年人,近端型好发于中老年人,男性多于女性,核心分子特征为 INI1(SWI/SNF 核心亚基)表达缺失。ES 恶性程度高、侵袭性强,易发生转移,对于不可手术的局部晚期或转移性经治患者,传统化疗疗效有限,现有靶向治疗选择匮乏,临床需求极为迫切。
在 2023 年 ASCO 大会上,艾普美妥司他治疗上皮样肉瘤患者首次人体 I/II 期研究中 I 期部分的初步结果首次亮相。
2021 年 12 月 2 日至 2022 年 11 月 7 日期间,来自中国 4 个中心的 32 名 ES 患者被纳入三个剂量组(400、600 和 800 mg BID)。前线治疗的中位数为 2 线。10(31.3%)名患者接受了≥3 线的前线治疗。31(96.9%)名患者的当地免疫组织学报告记录了 INI1 表达缺失。有 20 名(62.5%)患者为近端型。
400 到 800 mg BID 剂量组都观察到肿瘤应答。根据 RECIST 1.1,研究者评估的总体缓解率(ORR)为 28.1%。中位至缓解时间为 1.9 个月。一名完全缓解(CR)的患者从最初的缓解算起已经缓解了 273 天。疾病控制率(DCR)(DCR=CR+部分反应+疾病稳定 6 周)为 78.1%(95%CI:60-90.7)。
研究者评估的 艾普美妥司他在 400 mg BID 剂量的 ORR 和 DCR 分别为 36.4%(95%CI:10.9,69.2)和 81.8%(95%CI:48.2,97.7),在数值上高于总体人群。
截至 2023 年 2 月 28 日,中位治疗持续时间为 173 天,最常见的治疗相关不良事件(TRAE)是腹泻、血胆红素升高、皮疹、白细胞计数降低、贫血、尿胆红素升高、谷草转氨酶升高、低钾血症、高尿酸血症、谷丙转氨酶升高、脱发、血小板计数(PLT)降低。
≥3 级的 TRAE 包括腹泻、贫血和白细胞减少、低钾血症和中性粒细胞计数减少,以及血胆红素升高、PLT 降低、血肌酸磷酸激酶升高和高血糖症。没有 TRAE 导致的死亡。导致永久停药的 TRAE 仅在 1(3.3%)例患者中报告。分别有 25.0% 和 15.6% 的患者报告了导致剂量中断或减少的 TRAE。400 mg BID 剂量组在安全性方面优于整体数据。
Insight 数据库显示,在 EZH1/2 双重抑制剂赛道,目前全球范围内仅有第一三共的 Valemetostat 获批上市。除此之外,还有 5 款已经进入临床,来自诺华、海和药物、和黄医药、迪哲等,其中海和药物的艾普美妥司他是进展最快的,有望成为国产首款获批上市的 EZH1/2 小分子抑制剂。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..