3 月 10 日,CDE 官网显示,维昇药业递交的注射用那韦培肽拟纳入优先审评,适应症为适用于 2 岁及以上骨骺未闭合软骨发育不全儿童患者的治疗。
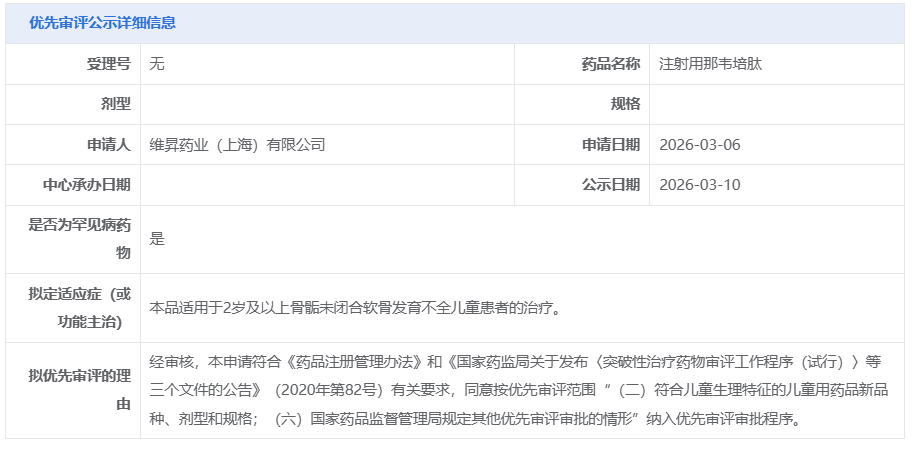
截图来源:CDE 官网
软骨发育不全症是一种罕见遗传性疾病,是侏儒症中常见的一种类型。该病由成纤维细胞生长因子受体 3(FGFR3)基因突变引发,会导致 FGFR3 与 C 型利钠肽(CNP)信号通路作用失衡,进而引发严重的骨骼并发症与合并症。临床前与临床数据显示,CNP 通路可调控生长发育,补充 CNP 能抵消 FGFR3 下游突变的异常影响,从而促进骨骼生长。
那韦培肽由 Ascendis Pharma 公司开发,维昇药业拥有那韦培肽在大中华区的独家开发、生产及商业化权利。作为 CNP 的研究性前药,那韦培肽采用每周一次的给药方式,其设计机制可向全身组织(包括生长板、骨骼肌)持续递送活性 CNP,以此实现对软骨发育不全症患者的治疗作用。
2 月 27 日,那韦培肽已获美国 FDA 加速批准上市,用于治疗 2 岁及以上患有软骨发育不全的儿童患者。此次批准是基于三项随机、双盲、安慰剂对照临床试验,以及长达三年的开放标签扩展研究数据,其中包括在软骨发育不全患儿中开展的关键性 ApproaCH 试验结果。
其中,ApproaCH 是一项关键的随机、双盲、安慰剂对照试验,ACH 患儿接受了 52 周的那韦培肽或安慰剂治疗,主要终点是 52 周时的年化生长速率 (AGV)。2025 年 7 月公布的 ApproaCH 试验 52 周结果显示:
那韦培肽组的 AGV 优于安慰剂,最小二乘 (LS) 平均 AGV 为 5.89 厘米/年,而安慰剂组为 4.41 厘米/年(LS 平均差 1.49 厘米/年,p<0.0001)。
安全性方面,那韦培肽组耐受性良好,约 99% 的报告不良事件为轻度(1 级)或中度(2 级)。无不良事件导致退出试验或停止治疗。两组治疗相关不良事件发生率相似。两组的 ISR(注射部位反应) 发生率均较低。所有 ISR 均为轻度(1 级)。在那韦培肽组和安慰剂组各有两名参与者记录了无症状低血压的不良事件,但均未被认为与治疗相关。
在中国,维昇药业已完成那韦培肽的 II 期临床试验,包括 52 周双盲治疗期及 52 周开放标签扩展阶段。研究结果显示,受试者以 100 µg CNP/kg/ 周的剂量治疗 52 周时,年化生长速率达 5.939 厘米/年,显著高于安慰剂组的 4.760 厘米/年。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..