5 月 7 日,CDE 官网显示,默克申报的氢溴酸尼罗司他片(Nirogacestat)拟纳入优先审评,用于需要系统性治疗的进展性韧带样纤维瘤病(也称为硬纤维瘤或侵袭性纤维瘤病)的成人患者。
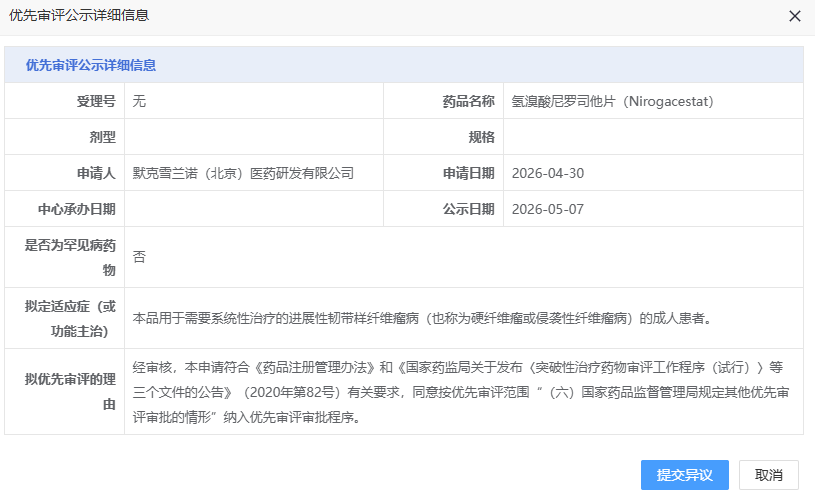
截图来源: CDE 官网
Nirogacestat(商品名:Ogsiveo)是一种 first-in-class 疗法,已获得美国 FDA 和欧洲药品管理局 (EMA) 批准上市,是治疗需要全身治疗的进展性纤维瘤成人患者的系统性标准疗法。默克于 2025 年 4 月以 39 亿美元收购SpringWorks Therapeutics 囊获了这款药物。
FDA 和 EMA 的批准是基于其 III 期 DeFi 试验的结果,该试验达到了改善无进展生存期(PFS)的主要终点,与安慰剂相比,疾病进展或死亡风险显著降低 71%(HR= 0.29)。Nirogacestat 组的中位 PFS 尚未达到,而安慰剂组为 15.1 个月。根据 RECIST v1.1 标准,Nirogacestat 组的确认 ORR 为 41%,而安慰剂组为 8%;Nirogacestat 组的完全缓解率为 7%,而安慰剂组为 0%。 Nirogacestat 组的中位首次缓解时间为 5.6 个月,安慰剂组为 11.1 个月。
无论基线特征(包括性别、肿瘤位置、肿瘤灶数、治疗状态、既往治疗、突变状态和家族性腺瘤性息肉病史)如何,Nirogacestat 组的 PFS 和 ORR 均优于安慰剂组。
Nirogacestat 展现出良好的安全性和耐受性。接受 Nirogacestat 治疗的患者中最常见的不良事件(发生率> 15%)包括腹泻、卵巢 毒性、皮疹、恶心、疲乏、口腔炎、头痛、腹痛、咳嗽、脱发、上呼吸道感染和呼吸困难。
另外,值得一提的是,Nirogacestat 还入围了 2025 年度盖伦奖最佳罕见病产品奖候选名单,该奖项被誉为「医药界诺贝尔奖」。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..