4 月 7 日,CDE 官网显示,吉利德「来那帕韦钠片」和「来那帕韦钠注射液」新适应症拟纳入优先审评,适用于与安全的性行为相结合,对于感染风险较高的成人和青少年(体重至少在 35kg 以上)进行暴露前预防,以降低通过性行为感染 HIV-1的风险。其中来那帕韦钠片为来那帕韦钠注射液的注射前口服导入用药,并用于在两次来那帕韦钠注射给药之间需要时进行口服桥接。
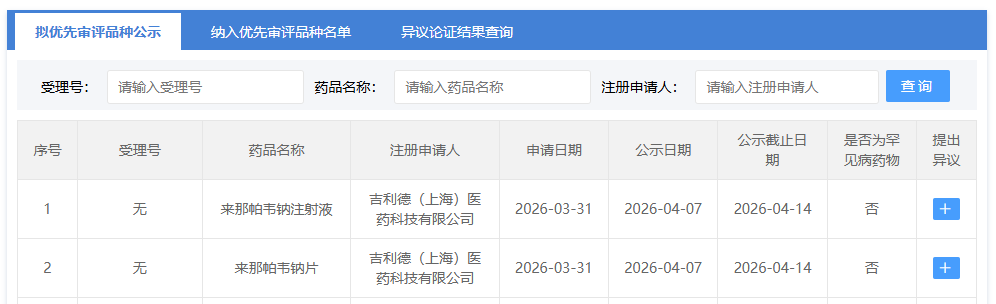
截图来源:CDE 官网
来那帕韦钠是一款全球首创的 HIV-1 衣壳抑制剂,通过直接结合病毒衣壳蛋白 p24 亚基,在 HIV 生命周期的多个关键阶段发挥作用:其既能抑制病毒逆转录过程,又能阻碍衣壳组装与拆卸,从而阻断病毒 DNA 进入细胞核及子代病毒释放。
因为采用缓释技术,来那帕韦钠注射液制剂可从注射部位缓慢释放,并维持有效浓度达 26 周,实现每半年一次的皮下给药。
此前,来那帕韦钠已在欧盟、美国、中国等国家和地区获批,联合其他抗逆转录病毒药物,用于治疗多重耐药 HIV 感染的成人患者。2025 年 6 月,FDA 正式批准来那帕韦钠新适应症上市申请,用于体重 35kg 以上青少年与成人的 HIV 暴露前预防,成为全球首款只需一年两次注射的 HIV 预防措施,也是全球首个覆盖治疗与预防全周期的长效 HIV 药物。
彼时 FDA 的批准是基于关键 III 期临床 PURPOSE 1 和 PURPOSE 2 的积极数据。
PURPOSE 1 试验(NCT04994509)是一项 双盲、随机、III 期非劣性研究。试验共纳入 5300 余名 16-25 岁顺性别女性及青春期女孩,参与者按 2:2:1 比例分配至来那帕韦钠组(每年两次注射)、Descovy 组(每日口服恩曲他滨/丙酚替诺福韦)和 Truvada 组(每日口服恩曲他滨/替诺福韦二吡呋酯)。该试验以背景 HIV 发生率(bHIV)作为主要对照指标,以 Truvada 作为次要对照指标。
PURPOSE 1 研究结果显示:在 2134 名接受来那帕韦钠的女性中, HIV 感染病例为 0 例,实现 100% 感染风险降低。一年两次的来那帕韦钠不仅优于 bHIV(主要终点,发病率为 2.41例/100人/年),而且也优于每日一次的 Truvada(次要终点),这两个终点的 p 值均小于 0.0001。在试验中,来那帕韦钠总体耐受性良好,未发现显著或新的安全性问题。
PURPOSE 2(NCT04925752)是第二项证明一年两次注射来那帕韦钠用于 HIV 预防的关键 III 期试验。这项研究在全球 88 个地点开展,纳入 16 岁及以上顺性别男性、跨性别者及非二元性别人群,受试者按 2:1 比例随机分配至来那帕韦钠组(每年两次注射)与 Truvada 组(每日口服)。
PURPOSE 2 研究结果显示:在 2179 名使用来那帕韦钠的受试者中,99.9% 的人未发生 HIV 感染,且在预防 HIV 感染方面优于每日一次口服 Truvada 治疗组。
总体而言,两项试验数据均显示,一年两次注射来那帕韦钠显示出良好的预防 HIV 感染效果,且总体耐受性良好,未发现显著或新的安全隐患。
值得一提的是,根据吉利德此前公布的价格,用于治疗的来那帕韦钠,第一年 42250 美元(约人民币 30.3 万元),此后每年 39000 美元(约人民币 28 万元)。而作为预防用药,吉利德公司在此前接受采访时表示,来那帕韦钠在美国的定价将为每人每年 28218 美元(约人民币 20.3 万元)。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..