4 月 7 日,CDE 官网显示,施维雅的 Vorasidenib 片拟纳入优先审评,用于携带异柠檬酸脱氢酶-1(IDH1)或异柠檬酸脱氢酶-2(IDH2)突变的 2 级星形细胞瘤或少突胶质细胞瘤成人和 12 岁及以上儿童患者的手术(包括活检、次全切除或全切除)后治疗。
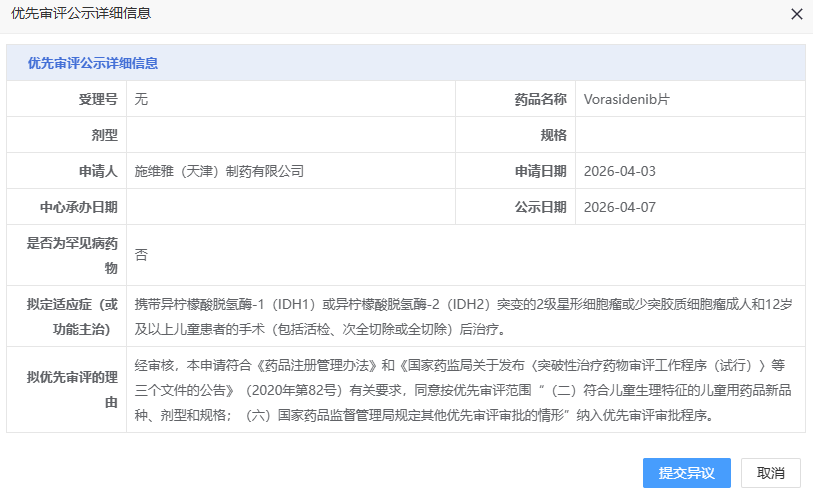
截图来源:CDE 官网
Vorasidenib 是施维雅在 2020 年通过收购 Agios 公司所得的一款口服、选择性、高度脑渗透性的双重抑制剂,2024 年 8 月,该药首次获得 FDA 批准上市,成为全球首个获批上市的 IDH1/2 双靶点抑制剂,也是近 20 年来 IDH 突变型弥漫性脑胶质瘤治疗领域首个创新靶点药物。
FDA 的批准是基于 III 期临床试验 INDIGO(NCT04164901)的积极数据。这是一项全球、随机、双盲、III 期临床试验,旨在患有 IDH1 或 IDH2 突变的残留或复发性 2 级少突或星形胶质瘤且仅接受过手术治疗的患者中,比较 Vorasidenib 与安慰剂的疗效,主要终点是 PFS。
试验数据显示,在 PFS 方面,Vorasidenib 单药治疗组患者的中位 PFS 为 27.7 个月,而安慰剂组为 11.1 个月;在关键次要终点下次干预的时间(TTNI)方面,Vorasidenib 组患者尚未达到中位 TTNI,而安慰剂组为 17.8 个月,两者具统计学显著性差异。
此外,Vorasidenib 单药治疗的耐受性良好。 最常见(≥15%)的不良反应包括疲乏、头痛、COVID-19 感染、肌肉骨骼疼痛、腹泻、恶心和癫痫发作。最常见的 3 级或 4 级实验室检查异常(>2%)包括丙氨酸氨基转移酶升高、天冬氨酸氨基转移酶升高、γ-谷氨酰转移酶升高和中性粒细胞减少。
而在国内,施维雅于 2024 年 7 月登记了一项 III 期、多中心、随机、双盲、安慰剂对照研究,旨在评估 Vorasidenib 治疗携带 IDH1 或 IDH2 突变的残留或复发性 2 级胶质瘤亚洲受试者的疗效和安全性。该研究的具体结果尚未披露。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..