4 月 7 日,CDE 官网显示,辉瑞申报的 1 类新药 PF-08634404 多项适应症获批临床,包括:1)联合化疗用于既往未接受过治疗的转化型小细胞肺癌的一线治疗;2)单药或联合治疗既往未接受治疗的局部晚期或转移性肾细胞癌。
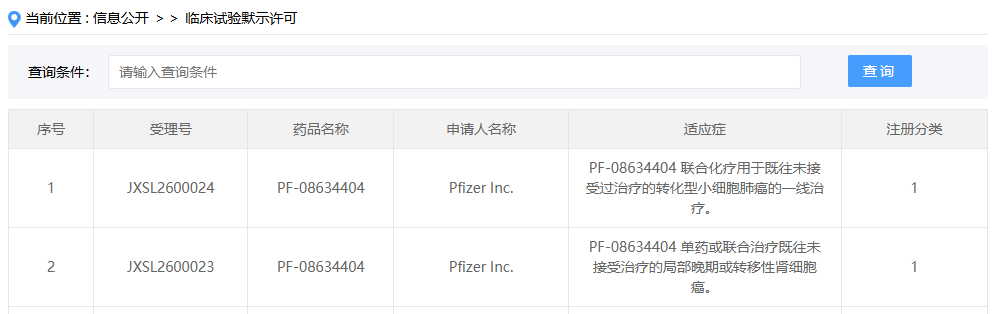
来源:CDE 官网
PF-08634404(三生制药研发代号:SSGJ-707)是三生制药开发的一款 PD-1/VEGF 双抗,2025 年 5 月,辉瑞以超 60 亿美元引进该产品全球开发与商业化权利,其中包括 14 亿美元首付款及 1 亿美元股权合作,一举刷新中国创新药单笔出海授权交易的首付款纪录。
依托于辉瑞的临床资源,PF-08634404 的临床进度正在高效推进中,已经开展 3 项 III 期临床试验,适应症包括结直肠癌、非小细胞肺癌,而计划开展的 III 期临床适应症还包括子宫内膜癌、尿路上皮癌等。
据 Insight 数据库统计,截至当前,国内已有 26 个 PD-(L)1/VEGF 抗体药已进入临床研发(获批临床及以上),依沃西单抗是全球首个且唯一获批上市的该类药物。
除此之外,还有 5 款 PD-(L)1/VEGF 抗体药已启动 III 期临床,包括 RC148(荣昌生物/艾伯维)、Sotiburafusp alfa(华奥泰)、SCTB14(神州细胞)、普密妥米单抗(BioNTech/BMS)和 PF-08634404(三生制药/辉瑞)。
值得一提的是,这 26 款已进入临床研发的抗体药物中还包括了 6 款三抗药物,来自华东医药、基石药业、宏成药业等。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..