3 月 20 日,CDE 官网显示,艾伯维乌帕替尼缓释片的一项新适应症上市申请获得受理,并被纳入优先审评,拟用于治疗成人和 12 岁及以上青少年的非节段型白癜风。如果本次申请获得批准,乌帕替尼将成为国内首个白癜风系统性靶向疗法。
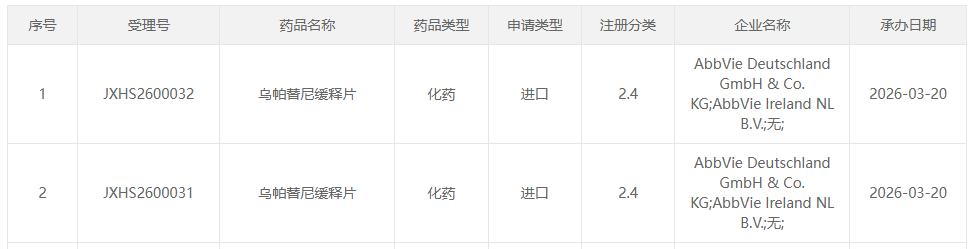
截图来源:CDE 官网
在国内,乌帕替尼此前已获批 8 项适应症,涵盖特应性皮炎、类风湿关节炎、银屑病关节炎、溃疡性结肠炎、克罗恩病、强直性脊柱炎、巨细胞动脉炎等。如果本次获得批准,将成为乌帕替尼在国内获批的第 9 项适应症。
2023 年 11 月,艾伯维启动了一项评价乌帕替尼在适合接受系统治疗的成年和青少年非节段型白癜风受试者中有效性、安全性和耐受性的 III 期、随机、安慰剂对照、双盲研究 Viti-Up。
Viti-Up 研究包括两项平行的 III 期研究(研究 1 和研究 2),每项研究均采用独立的随机分组、研究中心、数据收集、分析和报告机制。这些研究旨在评估适合接受全身治疗的成人和青少年 NSV 患者(12 岁及以上)中使用乌帕替尼的疗效、安全性和耐受性。共同主要终点是第 48 周时达到白癜风总面积评分指数 (T-VASI) 50(T-VASI 较基线改善 50%)、以及达到达到 F-VASI 75(F-VASI 较基线改善 75%)的受试者百分比。
研究结果显示,与安慰剂相比,乌帕替尼在第 48 周达到了共同主要终点 T-VASI 50 和 F-VASI 75。在两项研究中,在关键排序次要终点方面观察到乌帕替尼与安慰剂存在统计学显著差异,包括第 48 周时的 F-VASI 50。
安全性方面,两项研究中乌帕替尼的安全性特征与其在已获批适应症中观察到的安全性特征基本一致。未观察到新的安全性信号。
基于积极的 Viti-Up 研究结果,就在今年 2 月,艾伯维已向美国 FDA 和欧洲 EMA 提交了乌帕替尼用于治疗成人和青少年非节段型白癜风(NSV)的新适应症申请。
乌帕替尼是一种选择性 JAK 抑制剂,同时也是艾伯维旗下的重磅产品,2025 年全球销售额达到 83.04 亿美元( +39.07%)。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..