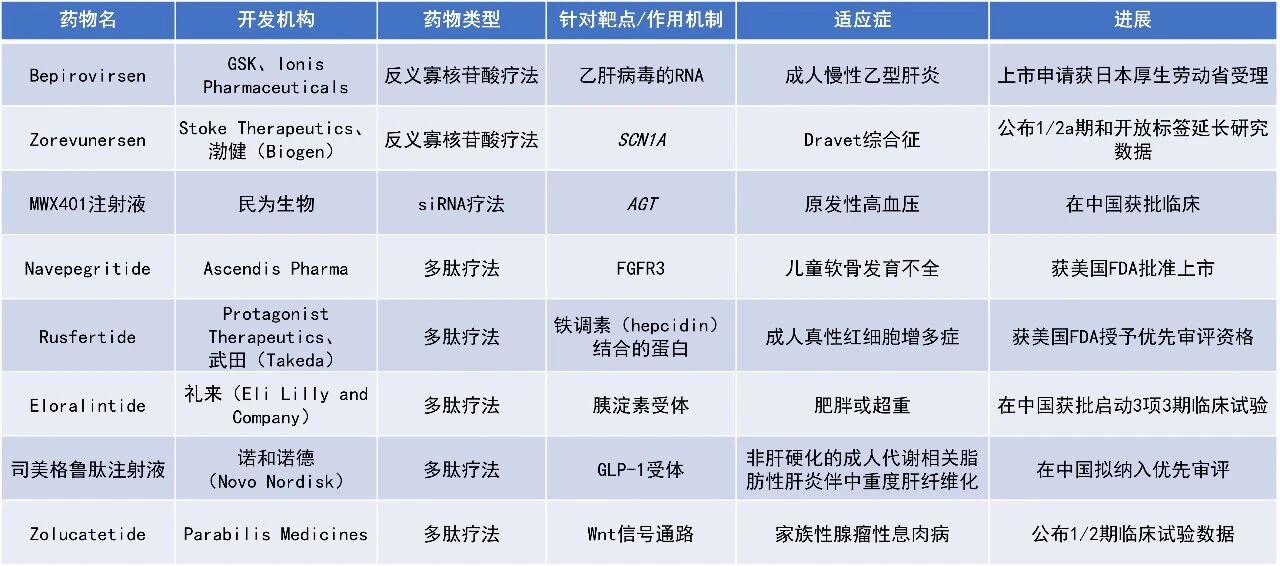
Bepirovirsen:上市申请获日本厚生劳动省受理 GSK近日宣布,日本厚生劳动省已受理其在研ASO疗法bepirovirsen的NDA申请,用于治疗成人慢性乙型肝炎。Bepirovirsen是一种具有三重作用机制的在研ASO疗法,旨在识别并靶向乙肝病毒的遗传成分(即RNA),从而可能使患者的免疫系统重新获得控制病毒感染的能力。Bepirovirsen可抑制体内病毒复制,降低血液中HBsAg水平,并激活免疫系统,从而提高获得持久应答的机会。GSK从Ionis Pharmaceuticals获得bepirovirsen授权,并与其合作推进该药物的开发。Bepirovirsen曾获得美国FDA授予的突破性疗法认定。 该申报基于B-Well1和B-Well2两项3期临床试验的积极结果。研究显示,与单纯标准治疗相比,bepirovirsen联合标准治疗在所有预设层级终点中均实现更高的功能性治愈率,且差异具有统计学意义和临床意义。其中,在基线乙肝表面抗原(HBsAg)水平较低的患者中观察到更为显著的疗效。同时,bepirovirsen展现出与既往研究一致的安全性和耐受性特征,整体安全性表现可接受。 Eloralintide:在中国获批启动3项3期临床试验 礼来宣布,其强效、选择性、AMYR激动剂eloralintide获中国国家药监局药品审评中心(CDE)批准,同步在中国开展3项全球性关键3期临床研究。这些研究将用于支持未来该产品在体重管理等多个适应症在中国的注册,以满足肥胖或超重患者及其相关合并症患者的临床需求,提供更多有效且耐受性良好的治疗方案。 Eloralintide能以高亲和力与人胰淀素1型受体结合,同时保持对人降钙素受体(hCTR)的选择性,在维持体重减轻效果的同时也改善了胃肠道反应,从而实现疗效和耐受性的平衡。Eloralintide对胰淀素受体的选择性可降低与降钙素受体活性相关的潜在风险。Eloralintide因其血浆半衰期较长(约14天),适用于每周一次皮下(SC)给药。 此前公布的2期研究LAA1结果显示,eloralintide所有剂量组均在体重降低和BMI改善等主要和多项次要终点上表现出较安慰剂具有临床意义的改善。相较于基线,在48周时eloralintide显示出显著的剂量依赖性体重下降,最高可达20.1%,平均腰围最大降幅17.1 cm。Eloralintide还与腰围、血压、血脂、血糖控制以及炎症标志物等多项心血管风险因素的改善相关。此外,在此研究中,所有剂量的eloralintide(1 mg、3 mg、6 mg和9 mg)均表现出良好的安全性和耐受。Eloralintide 9 mg(未进行剂量递增)显示出可接受的耐受性。采用3/6/9 mg剂量递增方案可进一步改善胃肠道不良事件。 Eloralintide正在开发用于作为饮食控制和运动的辅助治疗,单独用于肥胖或超重(合并至少1种体重相关合并症)的成人的长期体重管理;作为联合治疗,用于已使用稳定剂量肠促胰岛素类药物但未达到治疗目标的成人患者的长期体重管理。 司美格鲁肽注射液:在中国拟纳入优先审评 3月3日,CDE官网公示,诺和诺德申报的司美格鲁肽注射液新的上市申请拟纳入优先审评,拟定适应症为:治疗MASH伴中重度肝纤维化(符合F2-F3期纤维化)的非肝硬化成人患者。司美格鲁肽是一种胰高血糖素样肽-1(GLP-1)受体激动剂,它能够刺激胰岛素的生成,并抑制胰高血糖素分泌,降低食欲和食物摄入量。2025年8月,美国FDA加速批准Wegovy用于联合低热量饮食和增加体力活动,治疗伴有中度至重度肝纤维化(2期或3期)的非肝硬化型MASH成人患者。根据诺和诺德此前新闻稿,这是首个获批用于治疗MASH的GLP-1疗法。 FDA批准司美格鲁肽治疗MASH主要基于ESSENCE试验的第一部分结果,该结果已发布于《新英格兰医学杂志》。在第72周时,第一个主要终点数据显示,接受司美格鲁肽治疗的患者中,62.9%达到脂肪性肝炎缓解且肝纤维化未恶化,而安慰剂组为34.3%。两组间应答患者比例的估计差值(EDP)为28.7%。第二个主要终点显示,司美格鲁肽治疗组有36.8%的患者肝纤维化得到改善且脂肪性肝炎未恶化,而安慰剂组为22.4%。此外,第72周时的一个次要终点表明,接受司美格鲁肽治疗的患者中有32.7%同时达到脂肪性肝炎缓解及肝纤维化改善,而安慰剂组仅为16.1%。 Navepegritide:获美国FDA批准上市 Ascendis Pharma公司宣布,美国FDA已加速批准其多肽疗法Yuviwel(navepegritide;TransConCNP),用于治疗2岁及以上且骨骺尚未闭合的软骨发育不全儿童。Yuviwel是一种C型利钠肽(CNP)前体药物,每周给药一次,旨在提供患者活性CNP的持续暴露。C型利钠肽可通过阻断FGFR3的活性,从而解除对儿童生长的抑制作用,直接靶向软骨发育不全的病理生理机制,从而促进软骨内骨形成,让患儿的生长速率恢复正常。根据公司新闻稿,Yuviwel是首个获批用于该患者人群、每周一次给药的治疗方案。同时,该疗法也是目前首个能够在每周给药间隔期间实现持续性全身CNP暴露的软骨发育不全治疗药物。近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。日本厚生劳动省(MHLW)已受理GSK在研反义寡核苷酸(ASO)疗法bepirovirsen的新药申请(NDA),用于治疗成人慢性乙型肝炎(CHB)。礼来(Eli Lilly and Company)长效胰淀素受体(AMYR)激动剂eloralintide在中国获批启动3项3期临床试验。诺和诺德(Novo Nordisk)的司美格鲁肽注射液新的上市申请在中国拟纳入优先审评,用于治疗代谢相关脂肪性肝炎(MASH)伴中重度肝纤维化(符合F2-F3期纤维化)的非肝硬化成人患者。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..