8 月 13 日,CDE 官网显示,复宏汉霖和亿胜生物联合递交了贝伐珠单抗眼内注射液(HLX04-O)的上市申请。根据该药的临床研究进展推测本次申请适应症为:用于湿性年龄相关性黄斑变性。Insight 数据库显示,这是第 2 个在国内报上市的贝伐珠单抗眼科制剂。
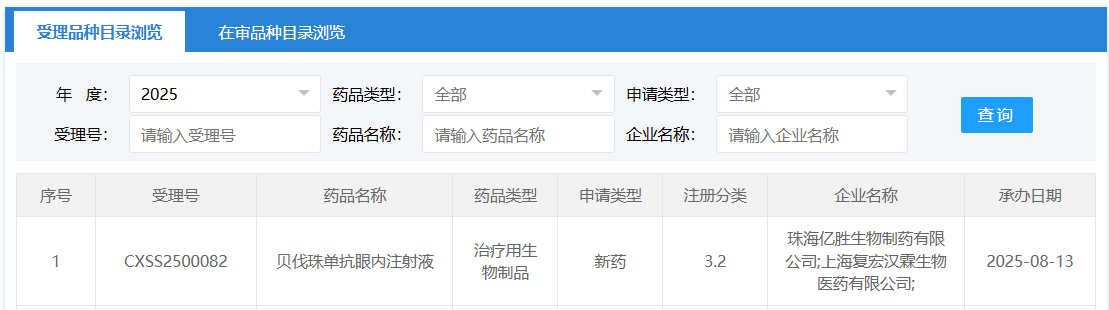
截图来源:CDE 官网
HLX04-O 是复宏汉霖利用基因工程技术构建的一款重组抗 VEGF 人源化单克隆抗体注射液,能够特异性结合 VEGF,阻断 VEGF 与内皮细胞上的受体 Flt1(VEGFR-1)和 KDR(VEGFR-2)结合,抑制其酪氨酸激酶信号通路的激活,进而抑制内皮细胞增生,减少新生血管生成,从而实现对 wAMD 等血管增生眼部疾病的治疗。
根据眼科用药需求,复宏汉霖在贝伐珠单抗汉贝泰®的基础上保持活性成分不变,对处方、包装材料、规格和生产工艺等进行优化,开发了新的眼科制剂产品 HLX04-O。可比性研究表明生产工艺和制剂处方的变更对药物制剂的质量、安全性和有效性未产生不利影响。
亿胜生物已和复宏汉霖达成协议,在全球范围内共同开发 HLX04-O 用于治疗湿性年龄相关性黄斑变性等眼科疾病。
2025 年 4 月,复宏汉霖宣布 HLX04-O 用于湿性年龄相关性黄斑变性 (wAMD) 中国患者的 III 期临床研究已成功达到预设的主要研究终点。这是一项多中心、随机、双盲、阳性对照的非劣效 III 期临床研究(NCT05003245),旨在比较 HLX04-O 与雷珠单抗玻璃体内注射(IVT)在 wAMD 患者中的有效性和安全性。研究的主要研究终点为第 48 周最佳矫正视力(BCVA)较基线改善的平均字母数变化,次要研究终点为其它有效性、安全性、耐受性及药代动力学指标。
研究结果显示,HLX04-O 组第 48 周 BCVA 较基线改善的平均字母数变化结果非劣于雷珠单抗组,达到主要研究终点。此外,HLX04-O 和雷珠单抗对 wAMD 患者人群整体、眼部、非眼部的安全性特征均相似,且安全性良好。
除 NCT05003245 外,复宏汉霖还就 HLX04-O 同步开展了一项国际多中心 III 期临床研究(NCT04740671),并在中国、澳大利亚、欧盟和美国等国家和地区入组受试者。
根据 Insight 数据库,国内尚无贝伐珠单抗获批治疗眼科疾病,也无贝伐珠单抗的眼科制剂获批。今年 6 月,兆科眼科和东曜药业联合提交了贝伐珠单抗眼科制剂 TAB014 的上市申请,用于治疗 wAMD 。复宏汉霖/亿胜生物的 HLX04-O 是第 2 款报产的此类药物。
四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..