6月25日,由盖茨基金会资助的独立调查新闻社(The Bureau of Investigative Journalism,TBIJ)发布报告,披露了一起令大众震惊而令研究人员“心碎”(heartbreaking)的全球性药品质量问题。报告显示,多个关键化疗仿制药未能通过质量检测,可能致使全球超100个国家的癌症患者面临治疗无效及潜在致命副作用的双重威胁。
这些药物涵盖治疗乳腺癌、卵巢癌、白血病等多种常见癌症的基础化疗方案,部分药物活性成分含量极低,几乎等同于无效治疗;而部分药物活性成分超标,可能引发严重器官损伤甚至死亡。TBIJ指出,这一事件不仅凸显了全球药品质量监管体系(尤其是WHO)的严重漏洞,更凸显了在药品质量把控、监管体系完善以及国际合作加强等诸多方面亟待解决的问题。
研究涉及七种常见抗癌药物:顺铂(cisplatin)、环磷酰胺(cyclophosphamide)、多柔比星(doxorubicin)、异环磷酰胺(ifosfamide)、亚叶酸(leucovorin)、甲氨蝶呤(methotrexate)和奥沙利铂(oxaliplatin),这些药物均被WHO列为基本药物。研究人员与喀麦隆、埃塞俄比亚、肯尼亚和马拉维的合作者一起,分析了来自这四个国家的药物样品。在189个未过期的样品中,约五分之一未能通过质量检测,涉及17家制造商生产的20种不同品牌仿制药。
不合格药物中,多数活性成分含量不足(大多数低于标签声明量的88%),部分则超标(超过112%)。其中质量问题最严重的是印度制药公司Venus Remedies生产的环磷酰胺,所有八个样品均未达标,其中六个样品的活性成分含量不足声明量的一半,一个样品仅含声明剂量的四分之一多一点,几乎等同于无效。
过去六年间,这些不合格品牌的药物已出口到全球的100多个国家(见下图),涵盖从尼泊尔、埃塞俄比亚、朝鲜等中低收入国家,到美国、英国、沙特阿拉伯等富裕国家。
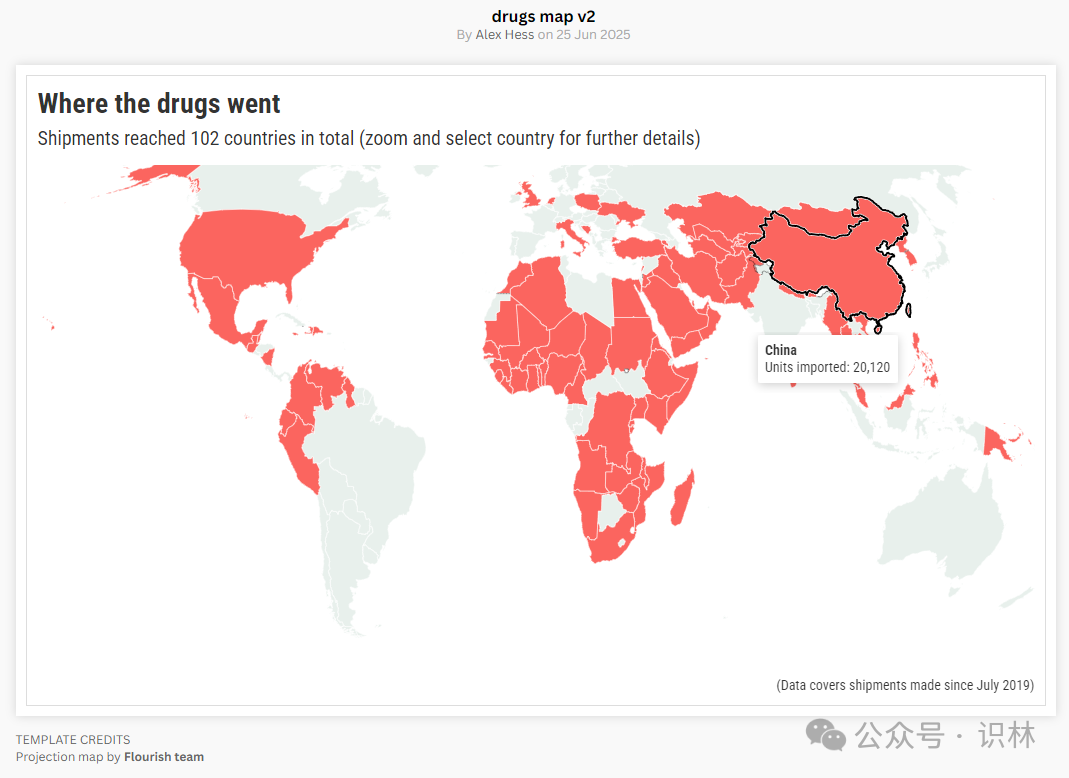
*报告附图,显示20120单位包装的相关药品进入我国。
印度药企问题最为严重。在此次调查涉及的17家不合格药物制造商中,有16家位于印度(1家来自突尼斯)。其中5家公司此前已被监管机构标记为生产过不合格批次的药物。Zee Laboratories自2018年以来已被标记46次。印度药品监管机构告诉TBIJ,Zee Laboratories已经接受了检查,并被下达了“停产令”。在公司解决了相关问题后该命令被解除。但监管机构没有透露这一命令是在何时下达的,涉及哪些问题,以及该公司是否面临任何后果。
与此同时,这些不合格的药物仍在药架上销售。Zuvius Lifesciences和GLS Pharma已将其不合格品牌供应给40多个国家。在过去两年中,Venus Remedies已获得一系列合同和许可证,包括从泛美卫生组织获得的向拉丁美洲国家供应几种基本抗癌药物的合同。
报告认为,价格驱动的仿制药市场造成了一个危险的局面,即生产某种药物的公司越来越少,直到全球供应危险地依赖于少数几家制造商。如果其中一家公司出现问题,数千名依赖这些药物的患者可能会受到影响。这种情况最近在美国就发生了。
在2018年至2022年期间,Intas制药公司(Accord Healthcare的母公司,其生产的顺铂在此次调查中表现最差)在美国的顺铂市场份额从24%增长到62%。在同一时期,该公司在甲氨蝶呤的市场份额也增加了五倍。与此同时,这两种化疗药物的价格都在下降。2022年底,FDA对印度的一家Intas工厂进行了突击检查,发现了一系列问题,包括员工被看到销毁质量记录。随后的停产在美国引起了连锁反应,据《纽约时报》报道,2023年春季或夏季,几乎美国所有的主要癌症中心都报告了化疗药物的短缺。
讽刺的是,在这种质量低下的竞争中,癌症患者往往是最终买单的人,尤其是在低收入国家,患者支付的费用最高:在这些国家,58%的基本抗癌药物费用由患者承担,而在中高收入国家,这一比例仅为1.8%。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..