12月3日,恒瑞医药宣布收到中国国家药品监督管理局(NMPA)下发的《受理通知书》,公司提交的JAK1抑制剂SHR0302片的药品上市许可申请获受理,本品适用于对一种或多种传统合成改善病情抗风湿药(csDMARDs)疗效不佳或不耐受的成人中重度活动性类风湿关节炎患者。
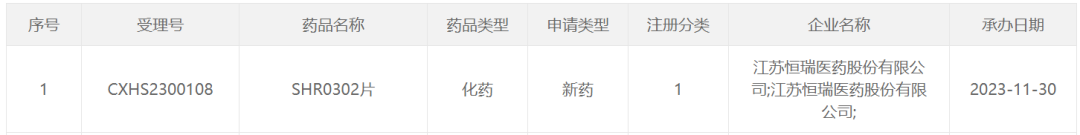
截图来源:中国国家药监局药品审评中心(CDE)官网
类风湿关节炎(RA)是以侵袭性、对称性多关节炎为主要临床表现的慢性、全身性自身免疫性疾病。RA的确切发病机制不明,目前认为主要由免疫系统攻击关节形成长期慢性炎症所致。目前RA治疗的总体目标是改善关节肿痛的症状、控制疾病进展、降低致残率、改善患者的生活质量。虽然已有较多类风湿关节炎治疗药物,但仍有部分患者使用现有药物治疗应答不佳或因无法耐受毒性反应终止治疗,亟需开发新的有效及安全的治疗药物。
SHR0302是恒瑞医药自主研发的高选择性的JAK1抑制剂,可通过抑制JAK1信号传导发挥抗炎和抑制免疫的生物学效应,并减少由于JAK2抑制引起的贫血等副作用。
据悉,SHR0302目前已开展了包括强直性脊柱炎、溃疡性结肠炎、特应性皮炎、斑秃、银屑病关节炎等多领域的临床研究,其中针对强直性脊柱炎和特应性皮炎的上市许可申请已获NMPA受理,其余绝大多数适应症的临床研究已进入3期临床试验。此外,该药用于轻中度特应性皮炎创新剂型的SHR0302外用软膏也已经进入3期临床。值得一提的是,2018年,恒瑞医药将JAK1抑制剂SHR0302许可给美国Arcutis公司。
根据恒瑞医药新闻稿,2023年9月,SHR0302片3期临床试验(SHR0302-301)达到了方案预设的主要研究终点。该研究是一项在传统合成改善病情抗风湿药反应不佳的中至重度活动性类风湿性关节炎受试者中评价SHR0302片疗效和安全性的多中心、随机、双盲、安慰剂对照的3期临床研究,由中国医学科学院北京协和医院曾小峰教授担任主要研究者,共入组566例成人中重度活动性类风湿关节炎患者。
该试验结果显示,SHR0302片8mg和4mg两个剂量组在主要终点上均显著优于安慰剂组,且在中重度活动性类风湿关节炎患者中长期治疗的安全性、有效性良好,与其他JAK1抑制剂相比未发现新的安全性信号。
参考资料:
[1]恒瑞医药创新药、JAK1抑制剂SHR0302类风湿关节炎适应症上市申请获受理. Retrieved Dec 3, 2023, from https://mp.weixin.qq.com/s/7xahSXE4UaKa7iLOOJ2W2A
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..