Abeona Therapeutics今天宣布,美国FDA已接受其在研疗法pz-cel(prademagene zamikeracel,EB-101)的生物制品许可申请(BLA),并授予优先审评资格,该疗法是一款自体、COL7A1基因校正表皮片,用于隐性营养不良性大疱性表皮松解症(RDEB)患者的治疗。美国FDA已设定该申请的PDUFA目标日期为2024年5月25日。
该BLA申请主要获关键3期VIITAL研究以及另一项1/2a期研究的临床疗效和安全性数据支持。两项研究均显示,在大型和慢性伤口上单次应用pz-cel治疗可实现持续伤口愈合和疼痛减轻。
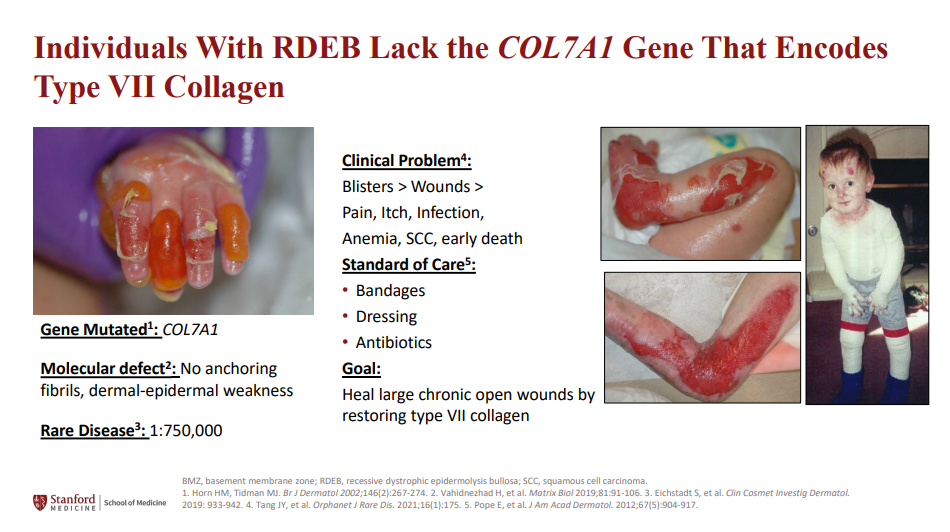
▲RDEB患者无法正常产生VII型胶原蛋白(图片来源:参考资料[2])
分析显示,该疗法在VIITAL试验中达成两项主要终点,大多数(81%)pz-cel治疗的伤口显示出≥50%的愈合程度,并且与对照伤口相比,pz-cel治疗的伤口中观察到疼痛严重程度有更大程度的减轻。即使对于较早的时间点,与对照伤口相比,使用pz-cel治疗的伤口显示愈合的百分比(≥50%、≥75%和完全)和疼痛严重程度的降低也更大。
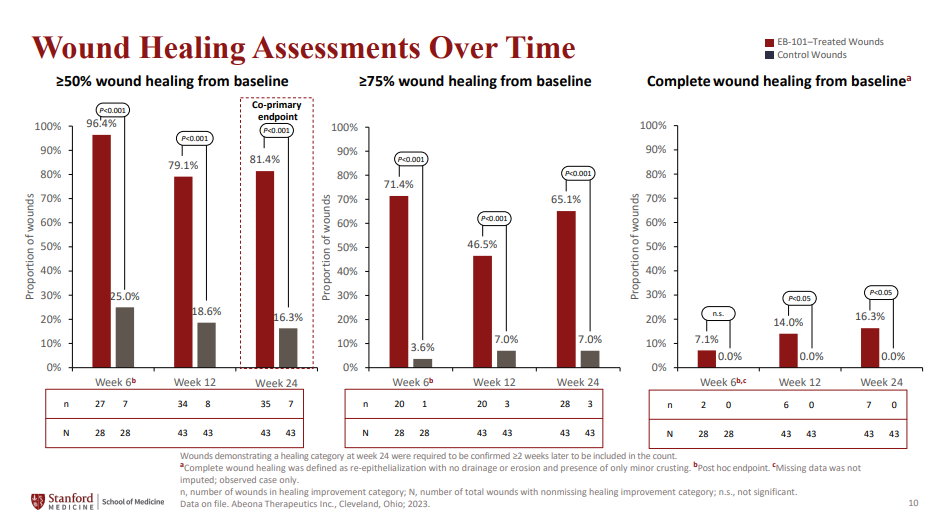
▲关键3期VIITAL试验疗效结果(图片来源:参考资料[2])
该疗法安全且耐受性良好,未报告患者水平或伤口特异性严重的治疗相关不良反应(TEAE),仅报告了少量非严重pz-cel相关TEAE,与既往临床试验结果一致。
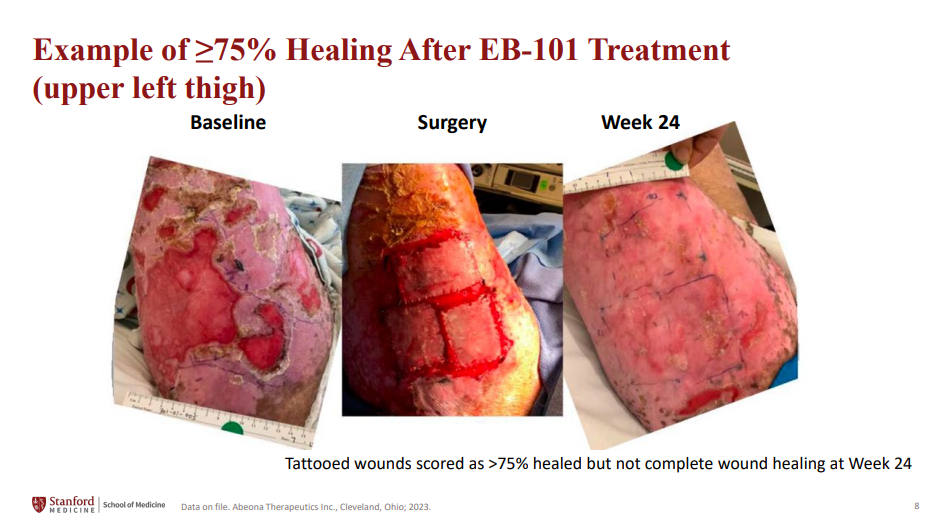
▲接受pz-cel治疗后,显示出≥75%愈合程度的伤口(图片来源:参考资料[2])
Pz-cel是Abeona的在研自体COL7A1基因校正表皮片,目前正在开发用于治疗RDEB,这是一种罕见的结缔组织疾病,由COL7A1基因缺陷引起,导致无法产生VII型胶原。Pz-cel旨在将功能性、产生胶原的COL7A1基因整合到患者自身的皮肤细胞中,并通过使用逆转录病毒载体稳定整合到分裂的靶细胞基因组中,实现长期基因表达。
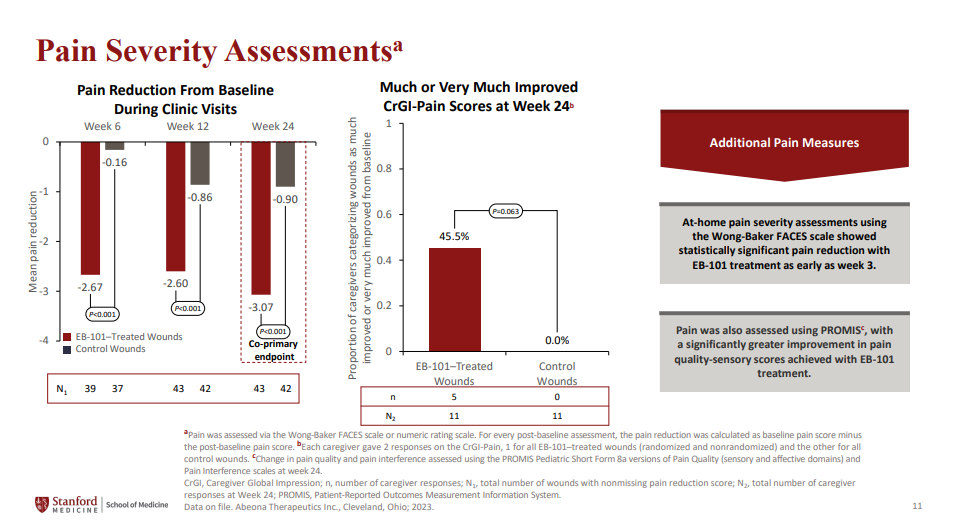
▲关键3期VIITAL试验疗效结果(图片来源:参考资料[2])
参考资料:
[1] Abeona Therapeutics Announces FDA Accepts and Grants Priority Review for Pz-cel Biologics License Application (BLA). Retrieved November 27, 2023 from https://investors.abeonatherapeutics.com/press-releases/detail/268/abeona-therapeutics-announces-fda-accepts-and-grants
[2] International Societies for Investigative Dermatology (ISID) Meeting. Retrieved November 27, 2023 from https://d1io3yog0oux5.cloudfront.net/_f9f4f56b4e0fc6c658b01f45fca61800/abeonatherapeutics/db/440/4098/presentation/VIITAL+ISID+2023+Oral+Presentation_Dr+Jean+Tang+Final.d3.pdf
四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..