9 月 25 日,据 Insight 数据库显示,罗氏萨特利珠单抗国内启动一项新 III 期临床,针对甲状腺眼病(TED)(登记号:CTR20232982)。

来自:Insight 数据库网页版(下文如无特殊标注,为同一来源)
萨特利珠单抗:
启动甲状腺眼病 III 期临床
萨特利珠单抗(Enspryng/satralizumab)是罗氏布局的一款 IL-6R 单抗。于 2020 年 8 月获 FDA 批准上市,用于治疗视神经脊髓炎谱系疾病(NMOSD)成人患者,此后,于 2021 年 5 月,在国内获批上市,成为国内首个视神经脊髓炎谱系疾病(NMOSD)治疗药物。
萨特利珠单抗全球项目开发进展
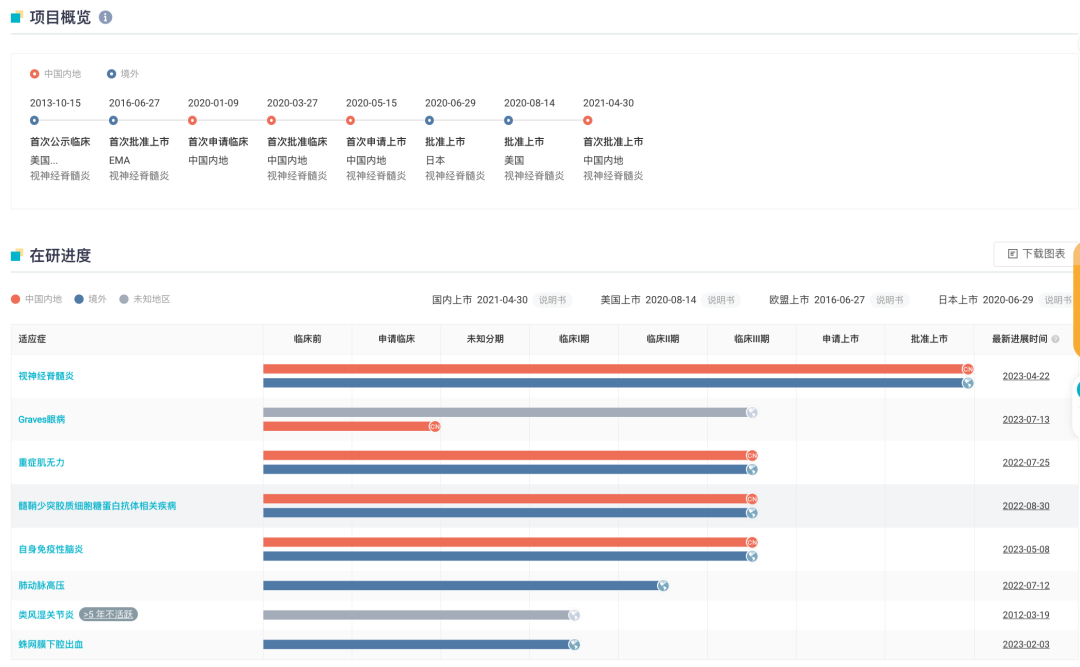
除视神经脊髓炎外,罗氏还在探索其他适应症,其中针对全身型重症肌无力(gMG)已处于 III 期临床阶段,其中,III 期 LUMINESCE 研究结果预计于 2024 年读出。此外,另有两项分别针对自身免疫性脑炎(AIE)、髓鞘少突胶质细胞糖蛋白抗体相关疾病(MOG-AD)的 CIELO、METEOROID III 期研究正在进行中。
而针对甲状腺眼病(Graves眼病/TED),据 9 月 11 日投资者活动日资料,罗氏在今年 Q3 登记启动 SatraGo-1、SatraGo-2 两项 III 期临床。
目前,据 Insight 数据库显示,罗氏 7 月在 ClinicalTriasls.gov 平台上登记了一项 III 期临床(登记号:NCT05987423),治疗中度至重度 TED 患者,目前入组 120 人,预计于本月底完成首例受试者的入组工作。在国内,7 月获批临床(受理号:JXSL2300071),并于今日启动临床。
单抗、基因疗法、ASO 疗法…
眼科后期管线齐上阵
在眼科领域,罗氏布局有多款潜在重磅产品。
明星产品 Faricimab(RG7716/法瑞西单抗/Vabysmo)是全球首款眼科双抗,采用罗氏专有 CrossMab 技术开发,可紧密结合 VEGF-A 和血管生成素 (Ang)-2。相较于既往眼科疾病当前常用的抗 VEGF 药,Faricimab 更长效。
作为 2022 年 1 月才获批上市的眼科药物,Vabysmo 2022 年全球销售额为 5.91 亿瑞士法郎,而 2023 仅半年就已达 9.57 亿瑞士法郎,挤入罗氏产品销售额前 8 名行列,增长强势,潜力巨大。罗氏预计 Vabysmo 2023 年销售额将超过 20 亿瑞士法郎。
从市场占有率来看,Vabysmo 2023 Q2 在美国的新生血管性年龄相关性黄斑变性(nAMD)市场份额达到 18%,糖尿病黄斑水肿(DME)市场份额达到 11%;且 1 年内在英国以及瑞士的市场占有率超过 20%。
目前,罗氏还在拓展 Vabysmo 新适应症,今年 5 月 FDA 已受理用于治疗视网膜静脉阻塞(RVO)的上市申请,PDUFA 目标审评日期为 12 月 22 日。
基于眼科巨大市场潜力,罗氏将进一步发挥其他眼科产品的潜力,除在积极推进萨特利珠单抗治疗甲状腺眼病(TED)的进展外,在后期管线中,罗氏还布局了 另一款 IL-6 单抗 RG6179 以及 Susvimo 等。
IL-6 单抗:RG6179
RG6179(RO7200220)是罗氏布局的另一款靶向 IL-6 单克隆抗体。当前正在针对葡萄膜炎性黄斑水肿(UME)以及 DME 进行临床开发。
RG6179 全球项目开发进度

此前披露的 I 期临床 DOVETAIL 研究结果为 RG6179 在葡萄膜炎性黄斑水肿(UME)患者中安全性和有效性研究提供初步数据。
基于此,去年 12 月罗氏同步登记了两项针对葡萄膜炎性黄斑水肿(UME)的 III 期临床 Meerkat、Sandcat 试验,前者于今年 1 月完成首例受试者的入组工作,后者为今年 3 月;并预计均于 2025 年读出相关数据。
其中,Meerkat 试验地区包含中国内地,并于今年 7 月登记启动了国内部分研究(登记号:CTR20232119);Sandcat 试验地区则不包含国内。
而针对 DME,则处于 II 期临床阶段。当前正在同步开展 BARDENAS、ALLUVIUM 两项研究,不过试验地区均不含国内。
Susvimo
雷珠单抗是一种血管内皮生长因子(VEGF)抑制剂,旨在结合并抑制 VEGF-A,VEGF-A 是一种已被证明在新血管形成和血管渗漏中起关键作用的蛋白质。
罗氏 Susvimo(雷珠单抗 PDS 给药系统)在患者眼中植入一个可以定期补充药物的移植体,其可在长达数月的时间里持续释放抗 VEGF 抗体雷珠单抗,潜在降低了与频繁眼部注射相关的治疗负担,并提高了疗效持久性。
2021 年 10 月,Susvimo 获 FDA 批准用于玻璃体内治疗先前对至少两次抗血管内皮生长因子(VEGF) 注射有反应的新生血管或湿性年龄相关性黄斑变性(nAMD)患者。然而,2022 年 10 月,由于生产问题,罗氏在美国自愿召回该产品。罗氏此前表示,已查明原因并解决了相关问题。
除 nAMD 外,Susvimo 在其他适应症的疗效也已获得验证。分别针对糖尿病性黄斑水肿(DME)、糖尿病视网膜病变(DR)的 III 期 PAGODA、PAVILLION 研究均已取得积极结果。
此外,罗氏计划将于今年 Q4 重启评估每 9 个月在 nAMD 患者中重新填充一次 Susvimo 的 IIIb 期临床 VELODROME 试验。
此外,细胞疗法、以及 ASO 疗法针对 GA 的临床开发进展已进入 II 期阶段。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..