近日,89bio公司宣布,美国FDA授予其在研疗法pegozafermin治疗非酒精性脂肪性肝炎(NASH)患者的突破性疗法认定(BTD)。该公司同时计划于2023年第四季度与监管单位讨论其NASH的临床3期试验。
NASH是一项严重、渐进式的肝病。因为在肝脏内过多的脂肪堆积而引起慢性炎症,进而造成肝渐进式地纤维化(瘢痕形成),最终导致肝硬化,甚至是肝衰竭、肝癌与死亡。对于NASH病患,晚期纤维化与产生肝脏相关疾病和死亡风险相关。直至目前为止仍没有获批用于治疗NASH的疗法。
Pegozafermin是一款开发用以治疗NASH与严重性高甘油三酯血症(SHTG)的成纤维细胞生长因子21(FGF21)类似物。FGF21是一种内源性代谢激素,可调节能量消耗以及葡萄糖和脂质代谢。Pegozafermin利用该公司专有的糖基聚乙二醇化技术,可延长天然FGF21的半衰期和优化生物活性。
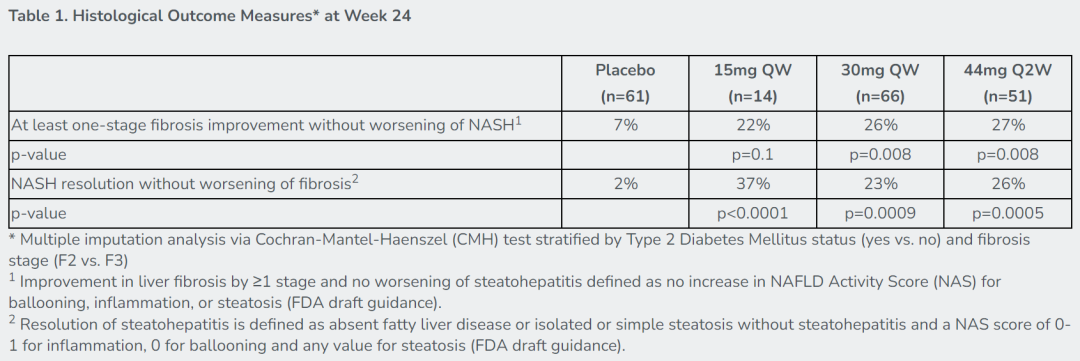
▲试验24周时,NASH患者的组织学检测数据(图片来源:参考资料[2])
这次突破性疗法认定的授予主要是基于在NASH患者中进行的ENLIVEN临床2b期试验数据的支持。分析显示,当患者接受每两周一次44 mg pegozafermin和每周一次30 mg pegozafermin时,均达成符合美国FDA指南的主要组织学终点,且具高度统计学显著性。此外,使用这两种剂量药物的患者还显示在肝脏脂肪、非侵入性肝纤维化和炎症标志物上具有统计学和临床意义的改善,以及在其他代谢和脂质标志物显示具有意义的改善。
在对这些数据的描述性分析中,45%的pegozafermin治疗患者在第24周时肝纤维化至少出现一个阶段的改善且NASH症状未恶化,而安慰剂组中的1例患者则没有出现改善。总体而言,pegozafermin通常具有良好的安全性特征,与既往研究一致。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..