5月24日,中国国家药监局药品审评中心(CDE)官网最新公示,罗氏(Roche)递交的恩曲替尼胶囊的新适应症上市申请拟纳入优先审评,拟用于NTRK融合阳性局部晚期或转移性实体瘤儿童患者。公开资料显示,恩曲替尼是一款靶向泛TRK及ROS1酪氨酸激酶的强效选择性抑制剂,已在中国获批治疗实体瘤、非小细胞肺癌(NSCLC)等适应症。
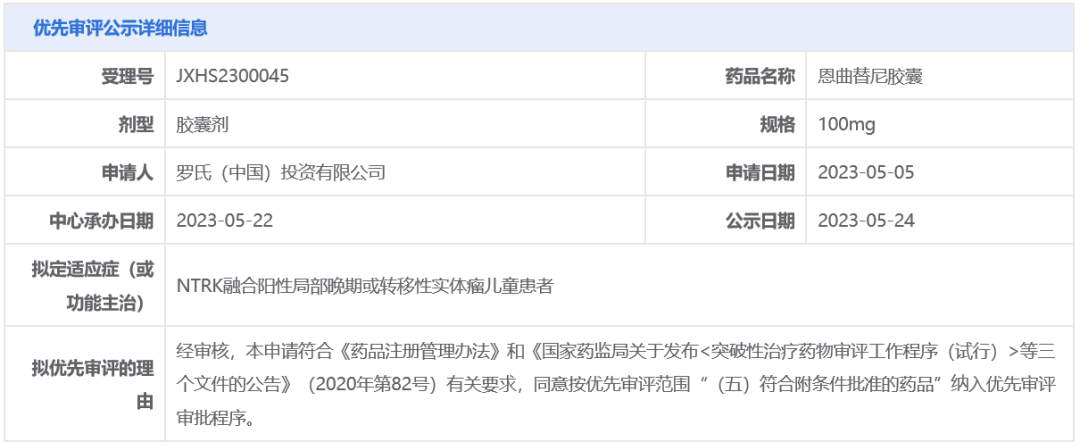
截图来源:CDE官网
恩曲替尼(entrectinib)是一款靶向泛TRK蛋白及ROS1酪氨酸激酶的强效选择性的抑制剂,具有中枢神经系统(CNS)活性,能够穿过血脑屏障,通过阻断ROS1和NTRK激酶的活性,造成ROS1阳性或NTRK阳性癌细胞死亡。2022年7月,恩曲替尼首次在中国获批,用于治疗携NTRK融合基因阳性实体瘤患者;2022年8月在中国获批用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌成人患者。
此次恩曲替尼胶囊的新适应症上市申请拟纳入优先审评,拟用于NTRK融合阳性局部晚期或转移性实体瘤儿童患者。NTRK基因融合是明确的致癌驱动因素,并在多个瘤种中表达,包括肉瘤、非小细胞肺癌和乳腺癌等,是泛肿瘤的潜在治疗靶点。有研究显示,实体瘤中NTRK基因融合的整体发生率为0.3%。
根据中国药物临床试验登记与信息公示平台,恩曲替尼有多项临床试验正在进行中,其中包括一项1/2期、开放性、剂量递增和扩展研究,旨在评估恩曲替尼用于治疗局部晚期或转移性实体瘤或原发性CNS肿瘤或未获得有效治疗的儿童患者的有效性和安全性。
此前,恩曲替尼已在一项名为STARTRK-NG的1/2期研究中取得积极结果,证明了该药用于21岁以下儿童和青少年NTRK、ROS1或ALK基因融合阳性的复发/难治性实体瘤患者的疗效。35例患者接受恩曲替尼治疗并进行疗效评估,中位年龄为7岁(4.9个月~20岁)。17例基因融合阳性者客观缓解率(ORR)为76%(13/17),其中原发性CNS肿瘤患者的ORR为70%(7/10),颅外实体瘤患者的ORR为86% (6/7)。恩曲替尼在儿童和青少年患者中的总体安全性与既往观察结果一致,试验中最常见的不良事件为贫血和体重增加。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.Retrieved May 24,2023, From https://www.cde.org.cn/main/xxgk/listpage/2f78f372d351c6851af7431c7710a731
[2]罗圣全®又一新适应症在中国获批!ROS1阳性非小细胞肺癌患者再获新希望. Retrieved Aug 15 , 2022. From https://mp.weixin.qq.com/s/HkTjwIclwt5ZXYJAH7KpIQ
[3]Ami V. Desai, et al. Updated entrectinib data in children and adolescents with recurrent or refractory solid tumors, including primary CNS tumors. 2020 ASCO Annual Meeting.
四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..