新冠疫情一轮又一轮肆虐,俨然已经成为了所有人生活中挥之不去的关键词之一。疫苗、中和抗体、小分子化药……药企和研究机构争分夺秒开发和迭代新药,以应对持续变化的疫情环境。
在已经过去的 2021 年度,辉瑞/BioNTech 的新冠疫苗以 367.8 亿美元的全球销售额荣登「药王」宝座,吉利德的瑞德西韦销售额也大涨 98%,收入 55.6 亿美元。随着 Paxlovid、Molnupiravir 等小分子药物的逐渐获批,其价值也将逐渐展现。 据 Insight 数据库,目前针对 COVID-19 的小分子化药开发在 3CLPRO、 RDRP 靶点密集扎堆,本文我们将简单概览 TOP 靶点们的研发进展。
全球在研 COVID-19 化药靶点分布情况
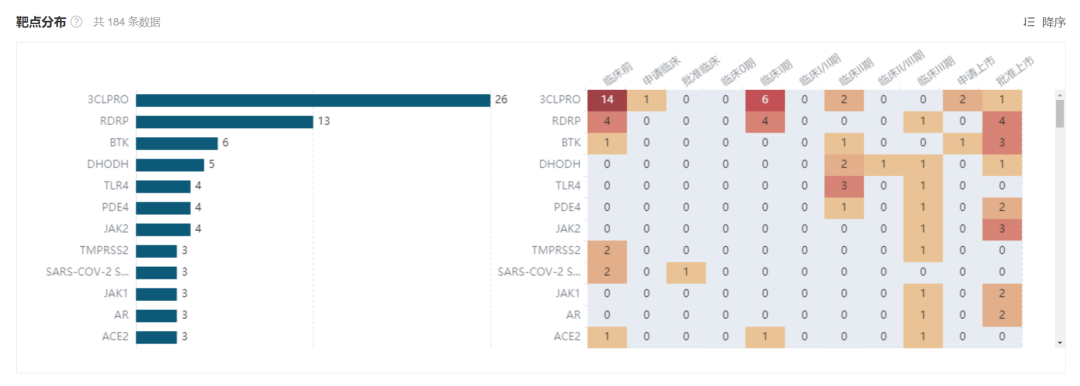
数据来自:Insight 数据库 全球新药(http://db.dxy.cn/v5/home/)
*仅筛选已有靶点披露的新药项目,不包括改良新和类似药/仿制药
3CL 蛋白酶
3CL 蛋白酶属于半胱氨酸蛋白酶,是新型冠状病毒复制必须的关键蛋白酶,且结构和功能较为保守,是抗新冠病毒小分子药物开发的重要靶点,相关小分子治疗药物具有效果好、广谱性、安全性好的优点。
这一靶点的典型代表是辉瑞的 PF-07321332,该成分与低剂量抗逆转录病毒药物利托那韦(Ritonavir)共同构成了口服复方制剂 Paxlovid 。Paxlovid 的疗效主要基于 3CL 蛋白酶抑制剂 PF-07321332 对新冠复制的抑制,利托那韦则用以减缓该成分的代谢或分解,使其在体内以更高浓度保持更长时间的活性。
Paxlovid 在去年 11 月公布了 2/3 期临床 EPIC-HR 研究数据,减少新冠肺炎非住院患者住院或死亡率 89%,一度引起轰动。12 月 22 日,美国 FDA 迅速对该药授予了 EUA 批准,用于高危成人和 12 岁及以上体重至少 40 公斤的高危儿科患者,这是该药全球首次获批;今年 2 月,国内 NMPA 也迅速批准 Paxlovid 进口。
尽管获批时间尚短,Paxlovid 已经成为业内乃至大众耳熟能详的重磅药物,其国内代理权、CMO 合作订单等都屡屡带来热议。这既基于 Paxlovid 突出疗效,也基于该药能给企业带来的极高收益。据辉瑞 2021 年报,预计 2022 年底将实现 1.2 亿疗程产能,实现超 220 亿美元的高收入。
据 Insight 全球新药库 显示,全球共 28 个 3CL 蛋白酶在研,除 Paxlovid 外,盐野义的 Ensitrelvir 也已经在日本提交了上市申请,另有 4 款药物处于临床 II 期开发,6 款药物处于临床 I 期开发。近期频繁的相关交易带来了早期临床前项目合作的不断涌现,15 个产品在临床前开发阶段,随时向临床试验发期冲击。
盐野义制药的 Ensitrelvir(S-217622)是仅次于辉瑞进度排位第 2 的 3CL 蛋白酶抑制剂,2022 年 2 月 25 日已经在日本提交上市申请。
据 Insight 数据库显示,Ensitrelvir 和其他新冠药物研发一样推进极快。盐野义在 2021 年 7 月启动了该药的 I 期临床(JPRN-jRCT2031210202),9 月启动 II/III 期临床(JPRN-jRCT2031210350),2022 年 3 月启动 III 期临床(NCT05305547)。盐野义表示,该药可单药给药,潜在疗效和安全性有望更优,公司已经推动 Ensitrelvir 的商业化生产,4 月份期实现 1000 万人份/年的产能。
而国内企业中,先声药业 2021 年 11 月与上海药物所合作引进了候选药物 SIM0417 ,在 2022 年 4 月 7 日启动 I 期临床;云顶新耀在今年 1 月超 2 亿美元从新加坡实验药物研发中心(EDDC)获得 EDDC-2214 的全球权益;君实生物合作苏州旺山旺水生物医药开发了 VV993;歌礼制药 ASC11 临床前数据也已公布,预计下半年递交 IND 申请……谁将脱颖而出成为首款上市来自中国药企的 3CL 蛋白酶抑制剂,让我们拭目以待。
RDRP
RNA 聚合酶抑制剂排位仅次于 3CL 蛋白酶抑制剂,靶点为 RDRP(RNA-dependent RNA polymerase),以默沙东的 Molnupiravir、吉利德的瑞德西韦(Remdesivir)、君实生物/旺山旺水的 VV116 为典型代表。这三款药物目前已经获批上市,其中 VV116 获批于乌兹别克斯坦。
Molnupiravir 公布临床数据早于辉瑞的 Paxlovid,两者几乎前后脚获批,不过其光环似乎被 Paxlovid 夺走,此前中期分析数据和最终数据的差异使 FDA 举行了咨询委员会专家会议投票以决定是否批准,最终 Molnupiravir 以 13:10 的优势赢得了批准。
瑞德西韦 在疫情之初则表现出新冠疗效,2020 年 10 月就获 FDA 批准。2021 年度瑞德西韦已经成为吉利德销售榜首,增长 98% 达到 55.6 亿美元。
国内 VV116 是开发进展最快的新冠口服药物,该药由君实生物和中国科学院上海药物研究所、中国科学院武汉病毒研究所、中国科学院新疆理化技术研究所、中国科学院中亚药物研发中心/中乌医药科技城(科技部「一带一路」联合实验室)、旺山旺水共同研发。目前,VV116 的 I 期临床数据已经公布,III 期临床试验也完成了首例给药,日前还启动了一项头对头 Paxlovid 的 III 期临床试验,足以体现企业对该药的信心。
据公开资料显示,VV116 临床前在体内外都表现出显著的抗 SARS-CoV-2 作用,对 SARS-CoV-2 原始株和已知重要变异株(Alpha、Beta、Delta 和 Omicron)均表现出抗病毒活性,同时具有很高的口服生物利用度和良好的化学稳定性。
不过,同靶点其他药物针对新冠肺炎的适应症开发大多集中在临床前。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..