5 月 11 日,药物临床试验登记与信息公示平台显示,和美药业登记了一项 1 类新药「莫米司特」(Hemay005)用于中度至重度溃疡性结肠炎(UC)患者的 III 期临床试验。
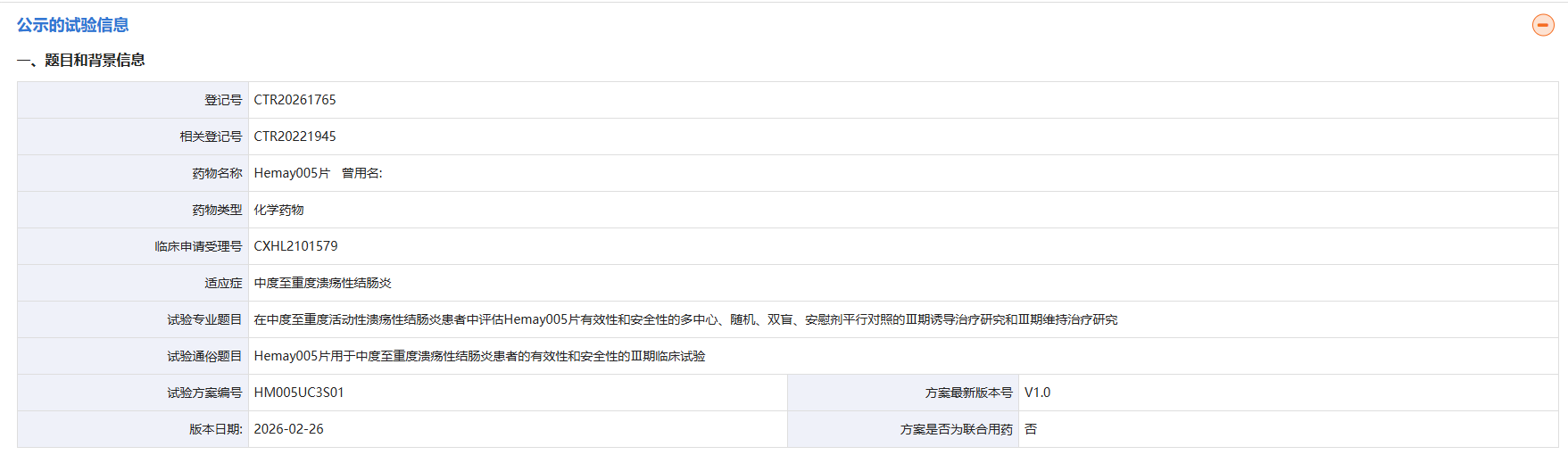
截图来源:药物临床试验登记与信息公示平台
这是一项多中心、随机、双盲、安慰剂平行对照的 III 期诱导治疗研究和 III 期维持治疗研究,拟在国内入组 360 人,主要目的是评估莫米司特在中度至重度活动性 UC 试验参与者中,诱导临床缓解和维持临床缓解的有效性。
莫米司特是一款磷酸二酯酶 4(PDE4)小分子抑制剂。据 Insight 数据库,该药早在 2013 年度就申报临床,2016 年公示启动首个临床试验,治疗银屑病;并于 2025 年 9 月首次获得 NMPA 批准上市,成为首款获批的国产 PDE4 抑制剂,首发适应症为斑块状银屑病。
除获批适应症之外,和美药业还在广泛探索莫米司特用于其他适应症的潜力,包括本次启动 III 期临床的 UC 适应症。其他适应症方面,关于白塞病的临床试验也已经推进到了 III 期、特应性皮炎、强直性脊柱炎两大适应症已完成 II 期临床。
结语
Insight 数据库显示,全球范围内共有 100 余款 PDE4 抑制剂在研(仅统计积极状态),适应症主要聚焦在银屑病、特应性皮炎、肺纤维化、慢性阻塞性肺病等。但在 UC 适应症方面,仅有 6 款 PDE4 抑制剂进入临床阶段,其中莫米司特是目前全球进展最快的产品。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..