3 月 30 日,阿斯利康宣布,中国 NMPA 已正式批准硫酸氢司美替尼胶适应症拓展,用于 3 岁及 3 岁以上伴有症状、无法手术的丛状神经纤维瘤(PN)的 1 型神经纤维瘤病(NF1)儿童及成人患者的治疗。
此前,司美替尼仅在国内获批用于该适应症的儿童患者,本次获批使其成为国内首个且唯一获批用于 3 岁及 3 岁以上 NF1-PN 患者的治疗药物。
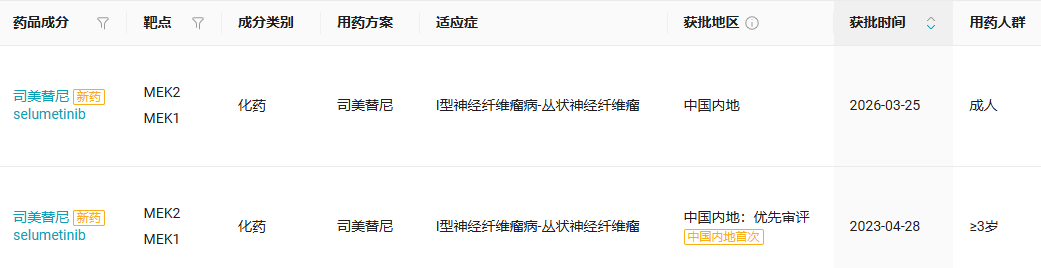
截图来源:Insight 数据库
NF1 是一种罕见的进展性、遗传性疾病,多在儿童早期确诊,病程常延续至成年,可导致全身多系统受累。多达 50% 的 NF1 患者会出现 PN,可累及大脑、脊髓以及周围神经系统,PN 也可能出现在患者的生命后期,并持续生长、体积增大,进而引发疼痛、外形畸形、肌肉无力等多种致残性症状。
司美替尼是一种选择性、口服 MEK 抑制剂,可阻断参与细胞生长刺激过程的特定酶(MEK1 和 MEK2)。在 NF1 中,这些酶活性异常增强,导致肿瘤细胞以不受调控的方式生长,从而形成所谓的丛状神经纤维瘤。通过阻断上述酶的活性,司美替尼可减缓肿瘤细胞的生长,从而减缓 PN 的生长。
此次获批是基于 Ⅲ 期临床试验 KOMET 的阳性结果。KOMET 是一项全球性 Ⅲ期、随机、双盲、安慰剂对照、多中心临床研究,旨在评估司美替尼在伴有症状且无法手术切除丛状神经纤维瘤的 NF1 成人患者中的疗效和安全性。该研究共纳入来自北美、南美、欧洲、亚洲及澳大利亚 13 个国家的 145 名成人患者,
新闻稿指出,KOMET 研究是 NF1-PN 成人患者中规模最大且唯一一项全球多中心、随机安慰剂对照 Ⅲ 期临床试验。中国亚组分析显示,在中国患者中观察到显著的临床获益,相关研究结果已于 2026 年 3 月 28 日在上海整形科技周上发布。
研究显示,在 KOMET Ⅲ 期临床研究的主要分析中,司美替尼组较安慰剂组显示出具有统计学显著性和临床意义的客观缓解率(ORR)。司美替尼的安全性与此前已知的安全性概况以及其在儿童患者中的既往应用经验一致。
基于 KOMET Ⅲ 期临床试验结果,司美替尼已在美国、欧盟、日本等多个国家获批用于治疗伴有症状且无法手术切除的 NF1-PN 成人患者,其他国家/地区的监管审查仍在进行中。
中山大学肿瘤防治中心,KOMET 研究中国牵头研究者陈忠平教授表示:成人 NF1-PN 患者往往面临着沉重的临床负担。司美替尼在儿科患者中的真实世界使用经验已充分证实其在儿童 NF1-PN 患者中的疗效;而作为全球首个针对伴有症状且无法手术的 NF1‑PN 成人患者开展的 Ⅲ 期临床试验,KOMET 研究进一步验证了司美替尼能够显著控制肿瘤进展、改善患者临床症状,并展现了良好的安全性。同时,在 KOMET 研究中,中国 4 个研究中心贡献了高质量数据,为全球研究成果提供了关键性支持。
目前,在NF1‑PN治疗领域,国内同靶点(MEK 抑制剂)产品为复星医药自主研发的芦沃美替尼片,今年1月申报拟纳入优先审评,用于伴有症状、无法手术的丛状神经纤维瘤(PN)的Ⅰ型神经纤维瘤病(NF1)成人患者。此外,处于临床阶段的MEK抑制剂包括诺华的曲美替尼(Trametinib,GSK1120212)、Arry/Pfizer的比美替尼(Binimetinib)、基因泰克/罗氏的柯美替尼(Cobimetinib)、海和药物 HH-2710、贝达药业 BPI-30000等。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..