日前,国家药品监督管理局药品审评中心(CDE)官网显示,君实生物自主研发的特瑞普利单抗注射液(皮下注射)的上市申请已获受理。这一进展意味着,我国肿瘤免疫治疗正逐步从传统的“静脉输注”模式向更为便捷的“皮下给药”模式迈进,国产PD-1的剂型创新竞赛也由此拉开新的序幕。
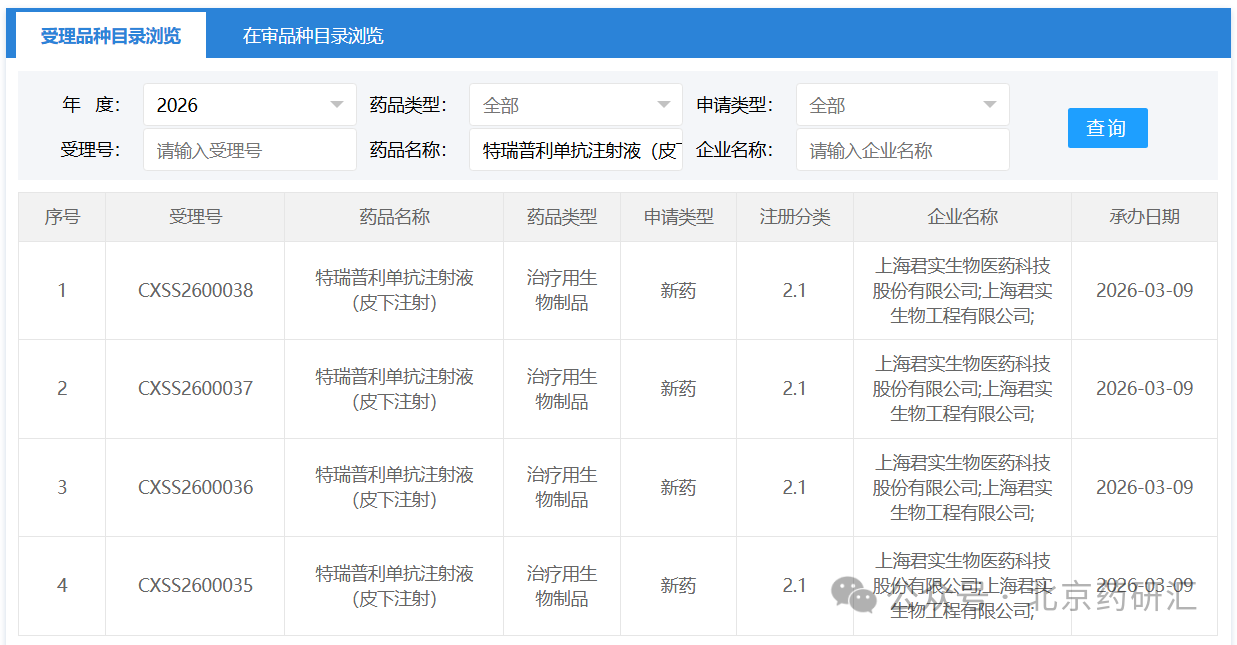
从全球范围来看,皮下注射PD-1/L1领域的研发已形成多梯队布局。截至目前,全球共有四款同类产品获批上市。君实生物此次率先在国内递交上市申请,不仅为患者提供了更为便捷的治疗选择,也标志着国产PD-1在剂型创新方面正逐步与国际前沿接轨,为我国肿瘤免疫治疗的差异化发展注入了新动力。
数小时输液到几分钟推注
治疗体验迎来重要改善
长期以来,肿瘤患者接受免疫治疗往往需要耗费数小时进行静脉输液。这一过程不仅需要建立静脉通路,对血管条件较差的患者而言更是一种额外的负担,而频繁往返医院也无形中增加了患者的就医成本。随着皮下注射制剂的问世,肿瘤免疫治疗有望从相对复杂的“住院模式”转向更为灵活的“门诊模式”,未来甚至有可能实现居家自我给药。
此次申报上市的特瑞普利单抗皮下注射制剂,是首个完成Ⅲ期临床研究并递交上市申请的国产PD-1皮下制剂。该剂型将原本需要30~60分钟的静脉输注时间,大幅缩短至仅需几分钟的皮下推注。这一改变不仅意味着肿瘤治疗可以像日常注射一样简便,也有望提升医疗资源的周转效率,同时在一定程度上改善患者的生活质量。
据了解,此次上市申请是基于一项多中心、开放、随机对照的Ⅲ期临床研究(JS001sc-002-Ⅲ-NSCLC研究)的积极结果。该研究由湖南省肿瘤医院邬麟教授担任主要研究者,旨在比较皮下注射特瑞普利单抗与静脉注射特瑞普利单抗联合化疗一线治疗复发或转移性非鳞状非小细胞肺癌的疗效和安全性。
临床研究数据显示,JS001sc在多个关键指标上与静脉注射制剂表现相当。研究结果表明,JS001sc的药物暴露量非劣效于静脉注射制剂,达到预设的统计学标准。在疗效方面,无论是客观缓解率、无进展生存期还是总生存期,皮下注射组均显示出与静脉注射组相似的获益趋势。这些循证医学数据为皮下制剂的临床推广应用提供了重要支撑。
在研发管线捷报频传的同时,君实生物近日发布的2025年度业绩快报,也为市场注入了一剂强心针。公告显示,公司全年营业总收入达到24.98亿元,较上年增长28.23%;虽归母净利润为-8.74亿元,但扣除股份支付影响后,亏损额同比大幅减少37.70%。这一显著“减亏”的背后,是公司“提质增效重回报”行动方案的深度落实。
公开数据显示,2022年至2024年,特瑞普利单抗在国内市场的销售额分别为7.36亿元、9.19亿元和15.01亿元,呈现逐年增长态势。进入2025年,这一增长势头愈发强劲,根据业绩快报披露,特瑞普利单抗注射液国内市场销售收入同比大幅增长约37.72%,成为公司营收增长的主要驱动力。
肿瘤免疫治疗赛道升温
步入剂型创新时代
在PD-1抑制剂适应症竞争日趋激烈的背景下,如何通过技术迭代实现差异化发展,已成为众多药企思考的重要课题。给药方式的优化,被认为是延长产品生命周期、拓展市场份额的有效路径之一。与此同时,随着部分重磅品种的专利期逐渐临近,开发便捷剂型也成为原研药企巩固市场地位的策略选择。
从全球范围来看,皮下注射PD-1/L1领域的竞争已呈多梯队布局态势。截至目前,全球已有四款皮下注射PD-1/L1药物获批上市:
罗氏的阿替利珠单抗(Tecentriq Hybreza)于2024年9月获美国FDA批准上市,该制剂将给药时间缩短至约7分钟。临床研究显示,患者偏好度较高,绝大多数患者更倾向于选择皮下注射方式。
百时美施贵宝的纳武利尤单抗(Opdivo Qvantig)于2024年12月获FDA批准,是全球首个获批的皮下注射PD-1抑制剂,其获批基于Checkmate-67T研究数据。该研究证实,皮下注射纳武利尤单抗在药代动力学和疗效上与静脉制剂相当,为临床提供了新的给药选择。
默沙东的帕博利珠单抗(Keytruda Qlex)于2025年9月获得FDA批准,是目前给药速度较快的皮下制剂之一,中位注射时间仅约2分钟。在针对一线非小细胞肺癌的临床研究中,皮下注射组展现出与静脉组相当的疗效,ORR为45.4%,略优于静脉组的42.1%。
思路迪/康宁杰瑞的恩沃利单抗作为全球首个获批的皮下注射PD-L1抑制剂,早在2021年即在中国获批上市,为肿瘤免疫治疗皮下给药积累了早期实践经验。
后续研发管线竞争同样激烈。辉瑞的Sasanlimab作为一种在研皮下注射PD-1抑制剂,目前已处于上市审评阶段;百济神州的替雷利珠单抗皮下制剂已进入Ⅲ期临床阶段;恒瑞医药、长春金赛等企业的同类产品也处于临床早期阶段,竞相探索差异化发展路径。
值得注意的是,君实生物计划在本次申报后,与监管部门沟通递交JS001sc用于特瑞普利单抗已获批的全部适应症的上市许可申请。公开信息显示,目前,特瑞普利单抗在中国内地获批上市的12项适应症,并全部纳入国家医保目录。这意味着,未来鼻咽癌、食管鳞癌、黑色素瘤等多个癌种的患者,均有望从这一便捷剂型中获益。
业内人士表示,随着特瑞普利单抗皮下注射制剂进入审评阶段,中国肿瘤免疫治疗的给药方式正在迎来新的变化。此次君实生物率先提交上市申请,不仅使国产PD-1在剂型创新方面与国际步伐保持同步,也为国内患者提供了更多元的治疗选择。在“用药便捷性”日益受到关注的当下,如何更好地为患者减负、提升治疗体验,或将成为未来市场竞争中的重要考量因素。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..