转自:CDE 排版:水晶
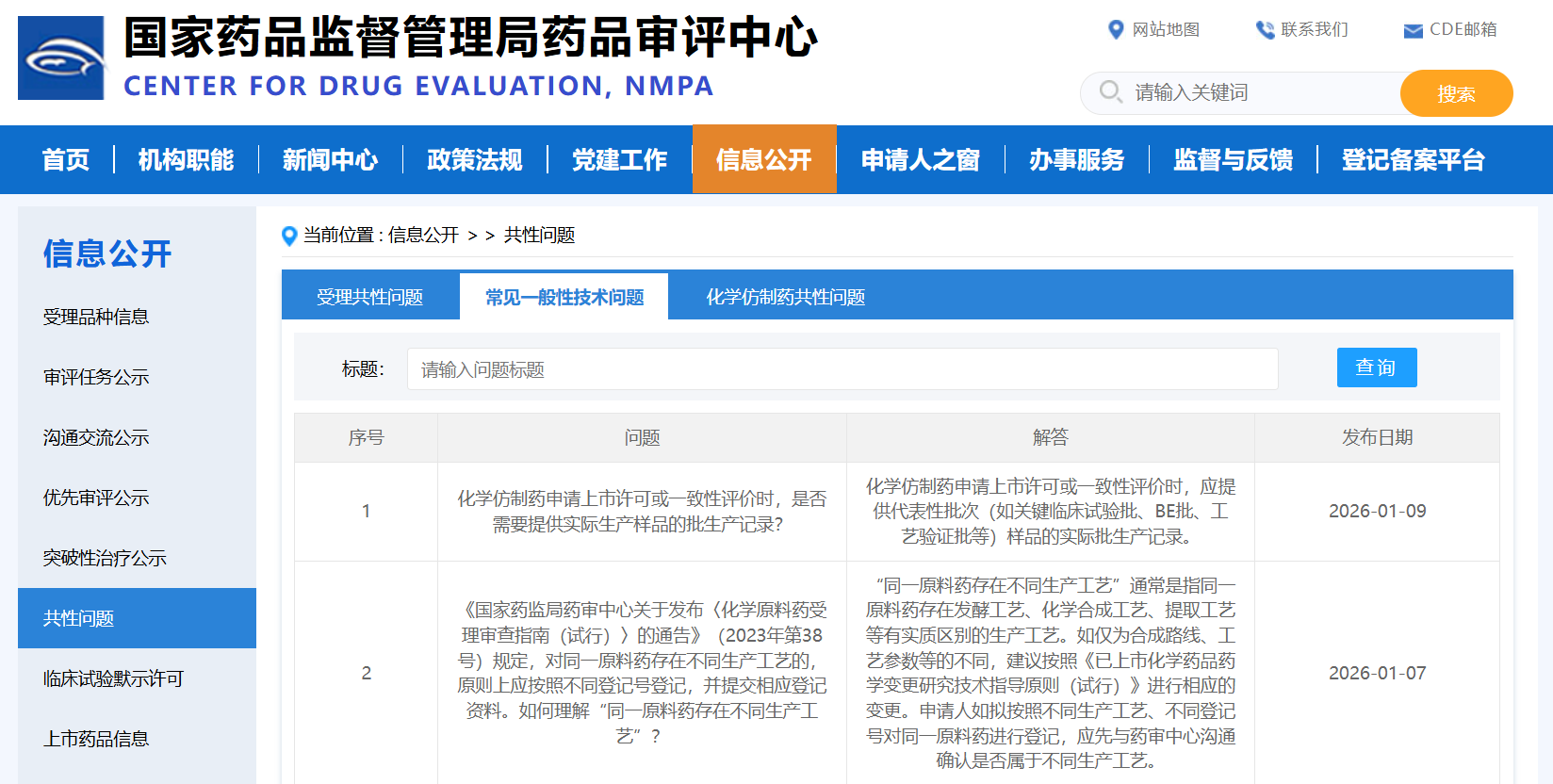
Q1:化学仿制药申请上市许可或一致性评价时,是否需要提供实际生产样品的批生产记录?
A1:化学仿制药申请上市许可或一致性评价时,应提供代表性批次(如关键临床试验批、BE批、工艺验证批等)样品的实际批生产记录。
Q2:《国家药监局药审中心关于发布〈化学原料药受理审查指南(试行)〉的通告》(2023年第38号)规定,对同一原料药存在不同生产工艺的,原则上应按照不同登记号登记,并提交相应登记资料。如何理解“同一原料药存在不同生产工艺”?
A2:“同一原料药存在不同生产工艺”通常是指同一原料药存在发酵工艺、化学合成工艺、提取工艺等有实质区别的生产工艺。如仅为合成路线、工艺参数等的不同,建议按照《已上市化学药品药学变更研究技术指导原则(试行)》进行相应的变更。申请人如拟按照不同生产工艺、不同登记号对同一原料药进行登记,应先与药审中心沟通确认是否属于不同生产工艺。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..