近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。阿斯利康(AstraZeneca)与Ionis Pharmaceuticals公司联合开发的反义寡核苷酸(ASO)疗法依普隆特生钠注射液在中国正式获批。石药集团的GLP-1/GIP受体双偏向性激动多肽SYH2069注射液首次在中国获得临床试验默示许可。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。
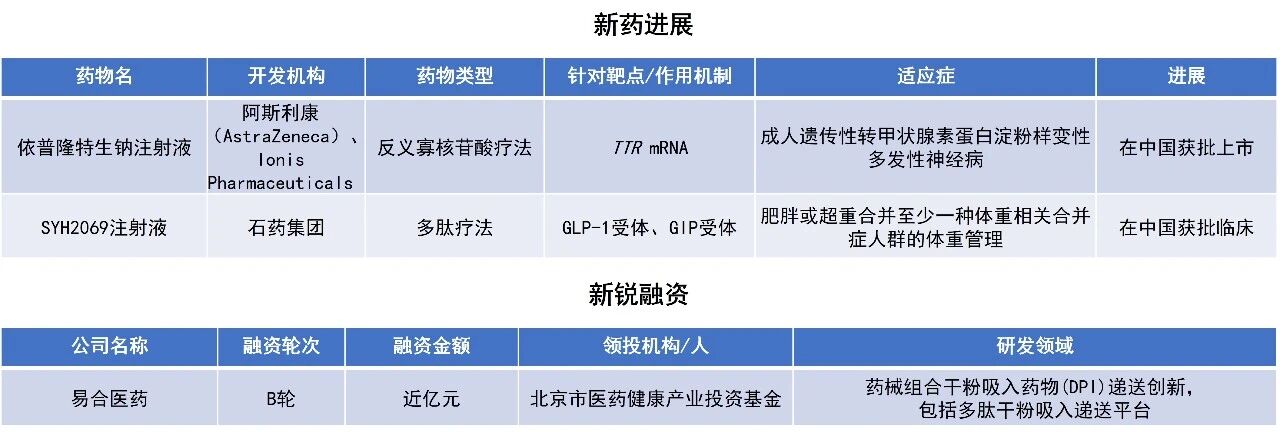
依普隆特生钠注射液:在中国获批上市
阿斯利康宣布,其与Ionis公司联合开发的万诺维(英文商品名:Wainua,通用名:依普隆特生钠注射液)在中国正式获批,用于治疗成人遗传性转甲状腺素蛋白淀粉样变性多发性神经病(ATTRv-PN)患者。依普隆特生钠(eplontersen)是一款ASO疗法,通过上游抑制转甲状腺素蛋白(TTR)的生成发挥作用。作为RNA靶向治疗药物,它可在肝脏源头减少TTR蛋白的产生,因而具有潜力用于治疗各类型的转甲状腺素蛋白淀粉样变性(ATTR)。该产品的获批,有望使此前治疗选择有限的患者能够通过自动注射器每月一次自行给药,显著提升用药便利性并改善生活质量。
中国国家药品监督管理局(NMPA)的批准基于NEURO–TTRansform 3期临床研究的积极结果。研究显示,在为期66周的观察中,与外部安慰剂相比,接受依普隆特生钠治疗的患者在两项共同主要终点(血清TTR浓度,以及以改良版周围神经损伤评分+7[mNIS+7]评估的神经病变损害)和关键次要终点(以Norfolk糖尿病神经病变生活质量问卷[Norfolk QoL–DN]评估的生活质量)方面,均表现出一致且持续的临床获益。该研究的积极结果已发表于《美国医学会杂志》(JAMA),进一步显示在治疗第35、66及85周,依普隆特生钠在ATTRv–PN的不同患者人群中均体现出获益。整个NEURO-TTRansform研究期间,依普隆特生钠持续展现出良好的安全性和耐受性。
SYH2069注射液:在中国获批临床
石药集团1类新药SYH2069注射液首次在中国获得临床试验默示许可,拟开发用于肥胖或超重合并至少一种体重相关合并症人群的体重管理。根据石药集团公开资料,这是一款GLP-1/GIP受体双偏向性激动多肽,其可选择性激活cAMP通路,显著降低β-arrestin募集,从而减少受体内吞及脱敏,提高药效和效果持续性。同时,结合长半衰期修饰平台技术,该产品能实现更深度、更持久的减重效果。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..