本期看点:
1. 抗体偶联药物(ADC)micvotabart pelidotin用于治疗复发/转移性头颈部鳞状细胞癌(R/M HNSCC)的1期临床试验结果积极,与pembrolizumab联合用于一线或二线及以上(1L/2L+)的患者时,客观缓解率(ORR)达71%,疾病控制率(DCR)为100%。
2. 线粒体质子载体TLC-6740联用GLP-1/GIP受体双重激动剂tirzepatide治疗肥胖,在一项早期临床试验中使受试者24周平均减重13.3%,且呈持续线性减重趋势,未导致瘦体重流失。
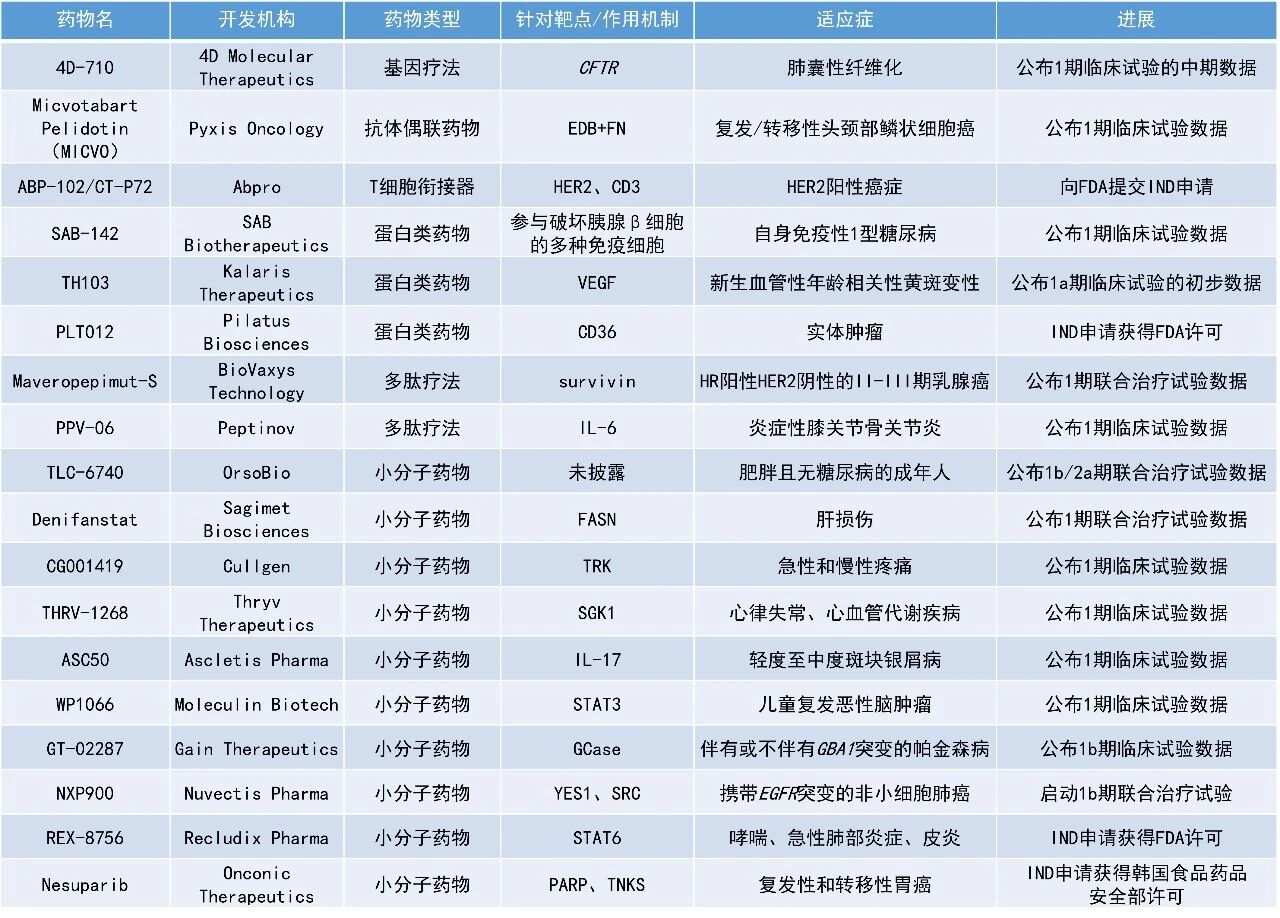
Micvotabart Pelidotin(MICVO):公布1期临床试验数据
Pyxis Oncology公司宣布,其ADC疗法micvotabart pelidotin(MICVO,原名PYX-201)用于治疗复发/转移性头颈部鳞状细胞癌的1期临床试验取得了积极的初步数据。MICVO以微管抑制剂(优化的auristatin)作为有效载荷,能靶向肿瘤细胞外基质(ECM)中的非细胞性结构成分——纤连蛋白B结构域(Extradomain-B Fibronectin,EDB+FN),通过直接杀伤癌细胞、降低细胞外基质密度、抑制血管生成及激活抗肿瘤免疫,实现多机制协同抗癌。该药已获美国FDA授予的快速通道资格,用于铂类和PD-(L)1抑制剂治疗后疾病进展的R/M HNSCC患者。
此次公布的结果显示,MICVO单药用于2L+ R/M HNSCC患者,确认的ORR为46%,DCR为92%。MICVO与pembrolizumab联合用于1L/2L+患者时,ORR提升至71%,DCR为100%。安全性方面,MICVO总体耐受良好,未观察到4级ADC有效载荷治疗相关不良事件,也没有观察到5级不良事件。
TLC-6740:公布1b/2a期联合治疗试验数据
OrsoBio公司宣布,其新型口服、肝脏靶向的线粒体质子载体TLC-6740在一项为期24周的1b/2a期临床试验中取得了积极的顶线数据。该研究评估了TLC-6740联合GLP-1/GIP受体双重激动剂tirzepatide治疗肥胖的效果。TLC-6740是一种新型口服药物,通过选择性作用于肝脏线粒体,增加能量消耗,旨在促进减重并改善代谢健康,包括改善胰岛素敏感性和脂质代谢。该药正在开发用于肥胖、糖尿病和代谢功能障碍相关脂肪性肝炎(MASH)等疾病。
此次公布的结果显示,在55名非糖尿病肥胖成人(平均BMI为37.5 kg/m2)中,联合治疗组(tirzepatide 5 mg+TLC-6740 180 mg)24周平均减重13.3%,较单用tirzepatide组患者(8.8%)额外多减重4.5%(约5.1公斤,相对提升51%,p=0.018)。此外,单药组在24周时体重下降趋于平台期,而联合组仍呈持续线性减重趋势。此外,TLC-6740联合tirzepatide的治疗显著改善了患者的胰岛素敏感性、肝脏健康和体成分,且未导致瘦体重流失。安全性方面,TLC-6740联用tirzepatide的安全性和耐受性良好,胃肠道不良反应与tirzepatide单药治疗相当。
SAB-142:公布1期临床试验数据
SAB BIO公司公布了其在研人类抗胸腺细胞免疫球蛋白疗法SAB-142的积极1期临床试验结果。SAB-142是一种人类多克隆免疫球蛋白,旨在治疗自身免疫性1型糖尿病。该药物可针对多种杀伤胰岛β细胞的免疫细胞,调节它们的活性,从而起到保护胰岛β细胞的作用。
此次公布的数据显示,SAB-142耐受性良好,未引发血清病(0/68),且无任何抗药抗体(ADA)相关不良事件(0/68),即使在再次给药的健康受试者中亦如此,表明其免疫原性极低或无免疫原性。所有受试者均未发生药物相关严重不良事件(SAE),大多数不良反应为轻度、短暂的1级类流感症状及输注部位反应。药效学方面,作为与靶点结合的标志,SAB-142诱导了短暂性淋巴细胞减少(100%受试者),但1–3天内即恢复至基线,恢复速度远快于其他免疫调节药物,支持其在门诊环境中的长期重复使用。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..