12 月 18 日,CDE 官网显示,和誉医药申报的 1 类新药 ABSK141 片获批临床,用于晚期实体瘤,包括但不限于结直肠癌、胰腺癌、肺癌等。这也是该药在国内首次获批 IND。
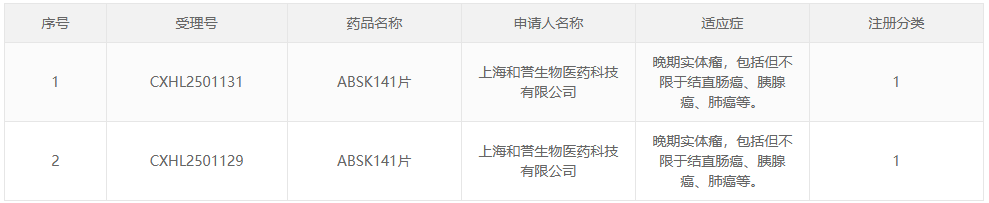
截图来源:CDE 官网
ABSK141 是和誉医药自主设计和开发的新型口服小分子 KRAS G12D 抑制剂,可以高选择性结合 KRAS G12D 突变蛋白,从而阻断下游信号通路,抑制肿瘤细胞增殖。
临床前研究结果显示,ABSK141 在多种动物模型中展现出潜在的同类最佳口服生物利用度,并在包括胰腺导管腺癌(PDAC)和结直肠癌(CRC)在内的多种人源肿瘤细胞系异种移植(CDX)模型中展现出显著的抗肿瘤活性。
2025 年 12 月 1 日,和誉医药宣布 FDA 已批准一项 ABSK141 的新药临床试验申请。这是一项开放性 I/II 期临床研究,旨在评估 ABSK141 在携带 KRAS G12D 突变的晚期实体瘤患者中的安全性、耐受性、有效性和药代动力学特征。
KRAS 是人类癌症中最常见的致癌驱动基因之一,其中 G12D 是最常见的突变亚型,广泛存在于 PDAC、CRC 及 NSCLC 等多种实体瘤中。由于 G12D 突变导致蛋白构象发生独特改变,其药物靶向性开发长期面临极大挑战,目前尚无针对 KRAS G12D 突变的靶向疗法获批上市。
Insight 数据库显示,全球目前共有 33 款 KRAS G12D 抑制剂进入临床阶段,其中恒瑞 HRS-4642、劲方医药 GFH375 进展最快,已进入临床 III 期,不过 HRS-4642 是注射剂型,GFH375 是口服片剂。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..