本期看点
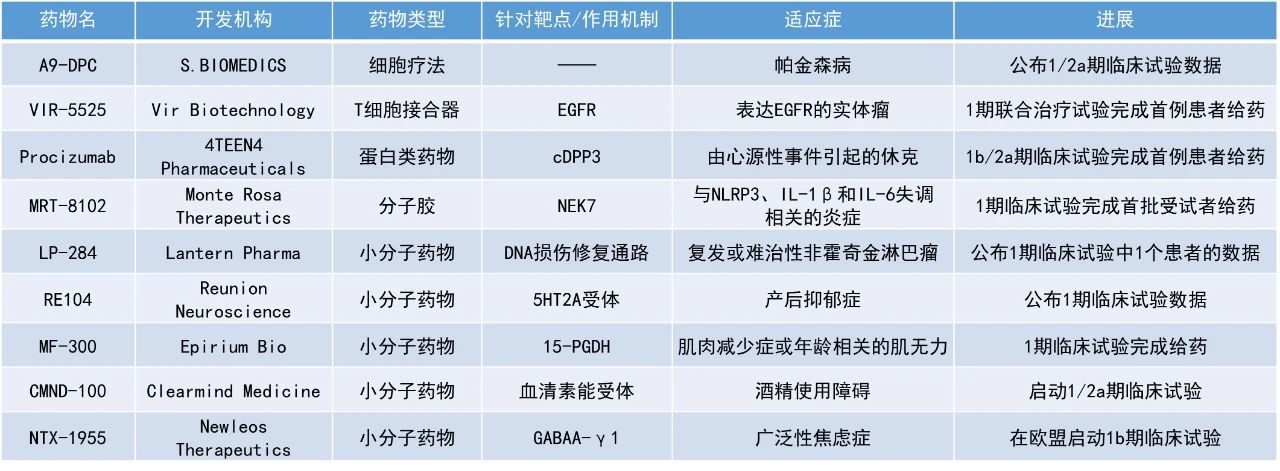
LP-284:公布1期临床试验中1位患者的数据
Lantern Pharma公司宣布,其在研疗法LP-284在一项1期临床试验中使1例此前接受过多种治疗的弥漫性大B细胞淋巴瘤患者实现了完全代谢缓解。LP-284是一种下一代酰基富烯(acylfulvene),通过合成致死机制靶向具有DNA损伤修复缺陷的癌细胞,拟开发用于治疗复发或难治性非霍奇金淋巴瘤及其他血液系统恶性肿瘤。该药物已获得美国FDA授予的多项孤儿药资格,包括套细胞淋巴瘤和高级B细胞淋巴瘤。
在该临床试验中,一名41岁、患有侵袭性3级非生发中心B细胞DLBCL的患者,在接受过三种先前治疗方案(包括标准化疗、CAR-T细胞疗法和双特异性抗体疗法)均告失败后,使用LP-284治疗仅两个周期(每个周期28天),便实现了完全代谢缓解。这是LP-284首次在临床中展现出完全缓解(CR)的效果,展现了其在治疗难治性侵袭性淋巴瘤和B细胞恶性肿瘤中的潜力。
NTX-1955:在欧盟启动1b期临床试验 Newleos Therapeutics公司宣布,将在欧盟启动其在研疗法NTX-1955治疗广泛性焦虑症的药理学和机制验证1b期临床研究。NTX-1955是一种潜在“first-in-class”的GABAA-γ1正变构调节剂,最初由罗氏(Roche)发现,目前正开发用于治疗GAD。GABAA是大脑中主要的抑制性神经递质,其受体的正变构调节已被证实是缓解焦虑症状的有效策略。非选择性GABAA PAM(如苯二氮䓬类药物)虽然具有显著的抗焦虑效应,但会广泛作用于全脑GABAA受体,包括那些介导认知障碍和镇静作用的功能区。相比之下,NTX-1955被设计为选择性调控杏仁核(大脑焦虑调节中枢,富含GABAA-γ1受体亚基)的GABA能神经传递,从而规避了苯二氮卓类药物相关的中枢神经系统安全性问题。 NTX-1955在多项标准临床前焦虑模型中展现出剂量依赖性的抗焦虑活性,其疗效与苯二氮卓类药物相当,但未出现经典苯二氮卓类药物的副作用。此外,NTX-1955已完成多项1期临床研究,证实该药物的安全性和耐受性良好,具有脑渗透性,并对GABAA-γ1具有选择性。
RE104:公布1期临床试验数据
Reunion Neuroscience公司宣布在The Journal of Clinical Psychopharmacology杂志上发表了其在研疗法RE104用于治疗产后抑郁症(PPD)的1期临床试验数据。RE104是一种致幻化合物,作为一款潜在“best-in-class”的4-OH-DiPT前药,它通过靶向血清素2A受体(5HT2AR)发挥作用。
在1期临床试验中,RE104的致幻活性与裸盖菇素(psilocybin)相似,但持续时间较短,只有3-4小时。在所有试验剂量下,RE104均表现出良好的安全性和耐受性。该公司评估RE104治疗中度至重度PPD成年女性患者疗效的2期临床试验数据预计将于2025年第三季度公布。
Procizumab:1b/2a期临床试验完成首例患者给药
4TEEN4 Pharmaceuticals公司宣布,其1b/2a期临床试验PROCARD1已完成首例患者给药。该试验旨在评估其选择性循环二肽基肽酶3(cDPP3)靶向单克隆抗体procizumab在主要由心源性事件引起的休克患者中的疗效。在生理状态下,DPP3是一种胞内酶,但在细胞损伤等病理情况下释放入循环系统后,会降解血管紧张素肽类物质,导致肾素-血管紧张素-醛固酮系统(RAAS)功能紊乱。这种RAAS调控失衡可引发休克、多器官功能衰竭乃至死亡。通过抑制cDPP3活性,procizumab能够恢复RAAS系统平衡并稳定心血管功能。临床前及临床试验结果表明,procizumab不仅能有效使患者的心血管参数恢复正常、逆转器官功能障碍,还可提高生存率。在已完成的一项针对健康受试者的1期临床试验中,procizumab还展现出良好的安全性和耐受性。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..