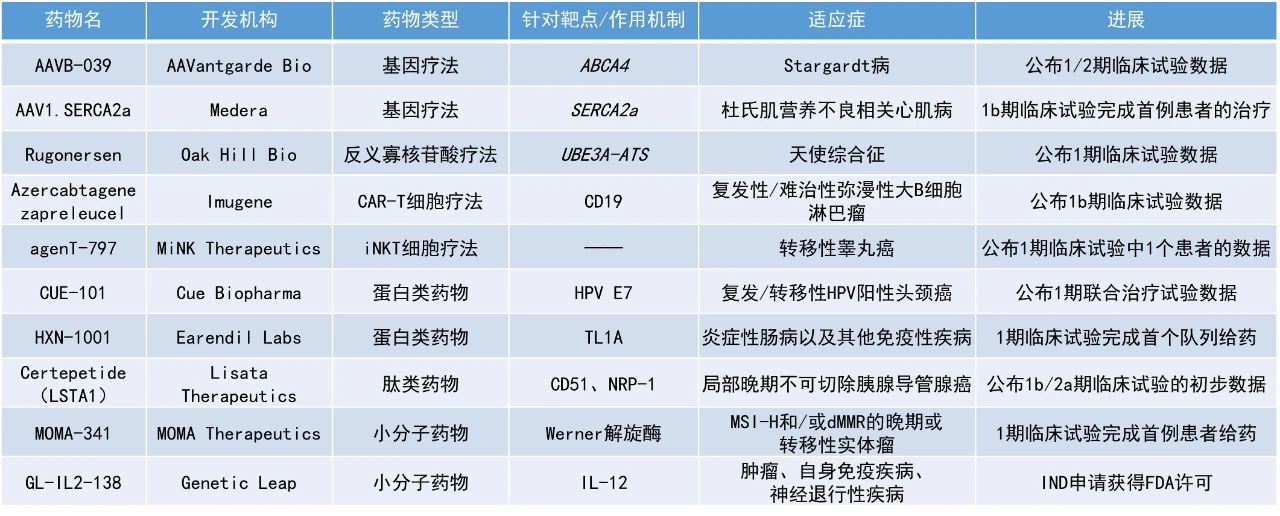
本期看点
CUE-101:公布1期联合治疗试验数据
Cue Biopharma公司公布了CUE-101治疗头颈鳞状细胞癌的1期联合治疗试验的积极新数据。CUE-101是该公司开发的一款基于IL-2的T细胞诱导剂,旨在选择性调节和激活HPV阳性T细胞,以提高疗效,同时减少传统免疫疗法的副作用。
截至2025年7月14日的数据,接受CUE-101联用PD-1抑制剂pembrolizumab一线治疗的HPV阳性复发性转移性HNSCC患者的客观缓解率(ORR)为50%,12个月时的总生存率为88%,中位OS为32个月。在历史研究KEYNOTE-048中,pembrolizumab单药治疗的ORR为19%,12个月时的总生存率为57%,中位OS为12.3个月。在肿瘤PD-L1表达综合阳性评分(CPS)≥1的患者中,2例患者达到完全缓解(CR),10例患者达到部分缓解(PR)。此外,接受该一线联合治疗的PD-L1低表达患者的ORR也达到了50%。
GL-IL2-138:IND申请获得FDA许可
Genetic Leap宣布,其新型小分子IL-2调节剂GL-IL2-138的IND申请已获得美国FDA许可。GL-IL2-138是一种小分子药物,通过结合内源性的IL-2 mRNA,促使免疫细胞系统性地产生天然IL-2蛋白。传统的重组IL-2蛋白(rIL-2)在临床上有重要地位,但由于毒副作用大、改良困难,IL-2曾一度被视为是“难以成药”的靶点。相比之下,GL-IL2-138具有更强的效力和持久性,并可通过口服方式给药,耐受性更高。此外,它具备广泛的应用潜力,涵盖肿瘤、自身免疫疾病及神经退行性疾病等多个领域。该药物即将进入一项随机、双盲、安慰剂对照的1期临床试验,以评估其在人体中的安全性、药代动力学和药效学特性。
MOMA-341:1期临床试验完成首例患者给药
MOMA Therapeutics公司宣布,其旨在评估MOMA-341的1期临床试验已完成首例患者给药。MOMA-341是一种高度差异化、潜在“best-in-class”的口服共价Werner解旋酶抑制剂,具有新型化学支架。MOMA-341正在被开发为单药疗法,或与化疗或免疫治疗联合使用,用于治疗微卫星不稳定性高(MSI-H)和/或DNA错配修复缺陷(dMMR)的晚期或转移性实体瘤,包括结直肠癌、胃癌和子宫内膜癌等。由于Werner解旋酶是MSI-H/dMMR肿瘤细胞存活所必需的,这使其成为一个有前景的新兴药物靶点。MOMA公司预计在2026年年中初步公布单药治疗数据。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..