Zolgensma 是一款针对 SMA 的基因疗法,通过单次静脉注射即可实现持续的 SMN 蛋白表达,从而阻止疾病进展。这是诺华在 2018 年以 87 亿美元收购 AveXis 公司获得的产品,在 2019 年 5 月首次获 FDA 获批上市,用于两岁以下 I 型 SMA 患者。
此前诺华披露,其针对 Zolgensma 研发的总投入达到了 94 亿美元(约合人民币 669 亿元),研发成本巨大。相对的,Zolgensma 的定价也并不便宜,以每剂 210 万美元(约合人民币 1495 万元)的价格上榜「全球十大最贵药物」,位列第 7。
从销售额角度来看,Zolgensma 上市后第一季度销售额就达到了 1.6 亿美元,2021 年销售额高达 13.51 亿美元,2022 年销售额进一步上涨到 13.7 亿美元,2024 年销售额为 12.14 亿美元。
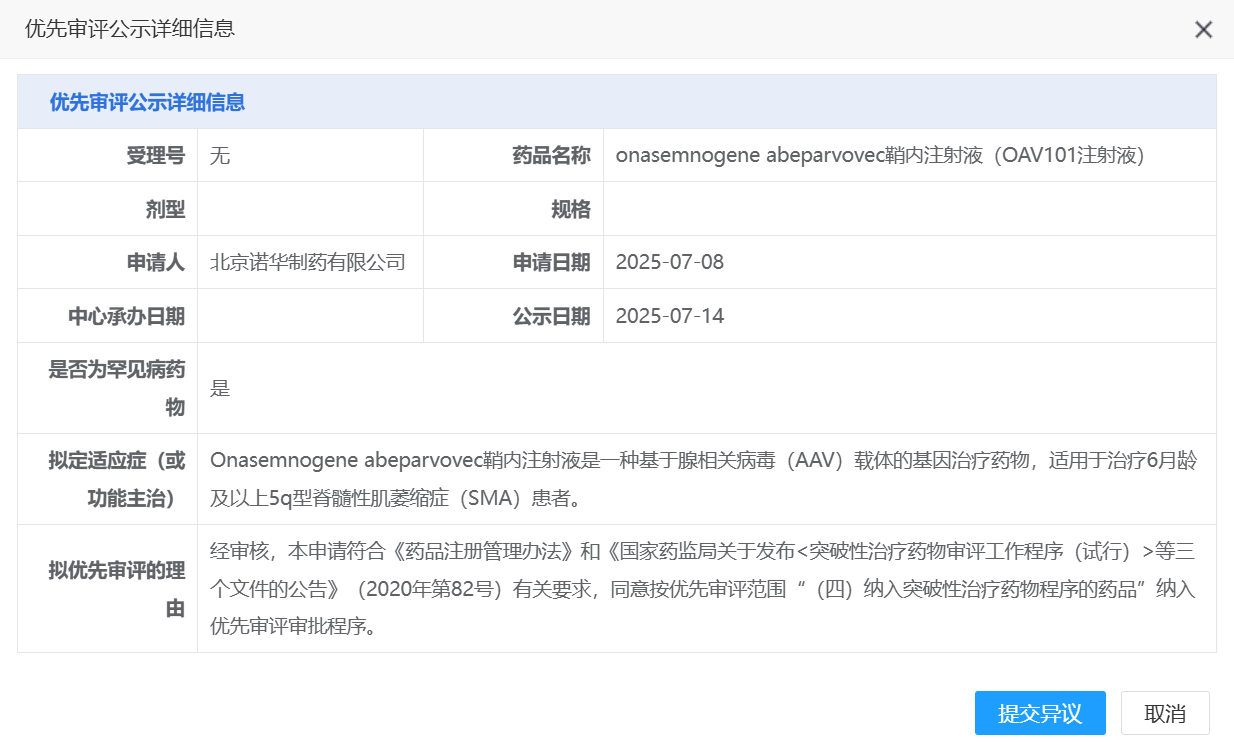
Insight 数据库显示,22 年 4 月,Zolgensma 首次在国内启动临床。这是一项随机、假操作对照、双盲、III 期临床试验,属于全球 III 期临床 STEER 研究(NCT05089656)的中国部分,针对 2 - 18 岁初治 2 型 SMA 患者,拟在中国入组 20 人,国际入组 125 人。
24 年 12 月,诺华宣布 STEER 研究达到主要终点。根据诺华新闻稿,这是首个在两岁及以上未接受治疗的 SMA 患者中具有临床获益的试验性基因疗法。
研究结果显示,相较于对照组,接受鞘内注射 Zolgensma 治疗的 SMA 患者的 Hammersmith 运动功能量表扩展版(HFMSE)总分较基线有所增加,这表明 SMA 患者的运动功能得到改善。详细数据将在 2025 年即将举行的医学会议上公布。
在安全性方面,Zolgensma 的安全性良好,两组之间的总体不良事件和严重不良事件相似。最常见的不良事件是上呼吸道感染、发热和呕吐。
Insight 数据库显示,目前全球范围范围内,SMA 新药仅获批 3 款,分别是 PTC Therapeutics 的利司扑兰、Ionis Pharmaceuticals 的诺西那生和诺华的 Zolgensma。值得一提的是,其余 2 款均为化药,仅诺华 1 款为基因治疗药物。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..