间质性肺疾病(ILD)是一组以肺间质炎症和纤维化为主要表现的异质性疾病,包括200多种可导致肺纤维化的肺部疾病。其中特发性肺纤维化(IPF)是代表性的肺纤维化ILD。除IPF以外的其他间质性肺疾病中,进展性肺纤维化(PPF)的定义为呼吸症状加重、生理监测中可观察到疾病恶化,以及影像学检查结果所证实的疾病进展。PPF不局限于特定基础疾病,很多类型的ILD均可能进展为PPF。尤其值得关注的是,类风湿关节炎、系统性硬化症等自身免疫性疾病一旦累及肺部,就可能发展为PPF,表现为进行性的呼吸道症状恶化和肺功能下降。由于PPF早期症状缺乏特异性,许多患者确诊时已进入快速进展期,预后不佳;在抗纤维化治疗上,手段也十分有限,患者的生存时间和生存质量亟待提高。
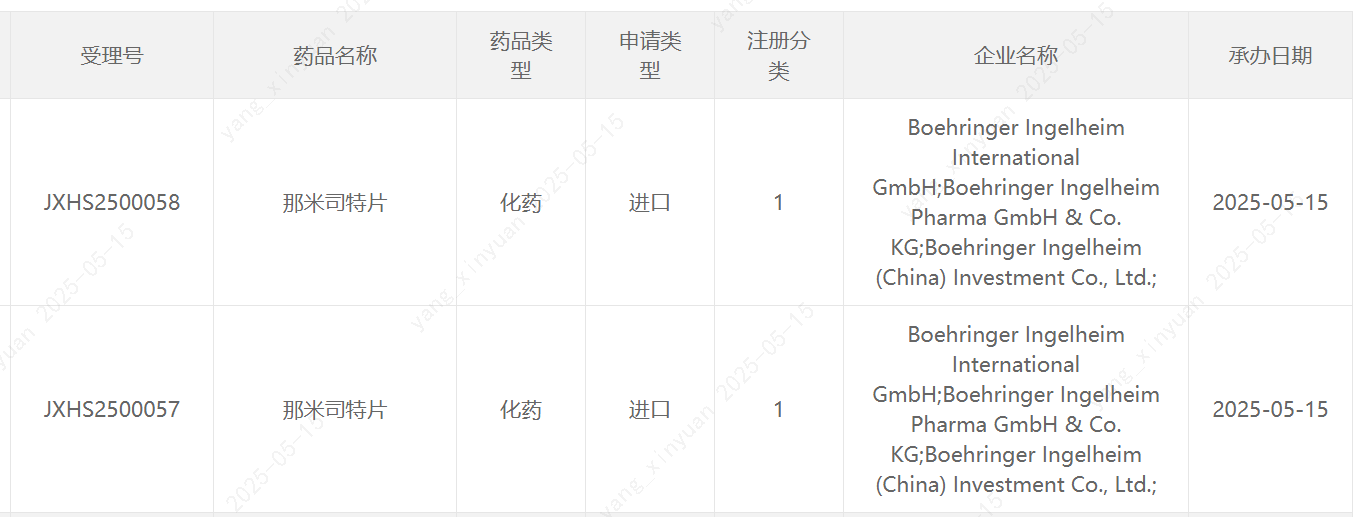
那米司特片是勃林格殷格翰在研的新型口服PDE4B选择性抑制剂,其通过抑制PDE4B发挥作用,该酶在肺部高度表达,并与纤维化和炎症过程密切相关。通过抑制这些通路,那米司特片展现了抗纤维化和免疫调节效应,有望为PPF患者带来临床获益。那米司特片正被开发作为IPF和PPF的潜在治疗药物。该产品已经获得美国FDA授予突破性疗法认定,用于治疗IPF和PPF。2025年,该产品治疗IPF适应症先后被FDA和中国NMPA纳入优先审评。
参考资料:
四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..