4 月 20 日,据 CDE 官网显示,百济递交的 1 类新药 BGB-B2033 临床试验申请获受理号(受理号:CXSL2400253)。
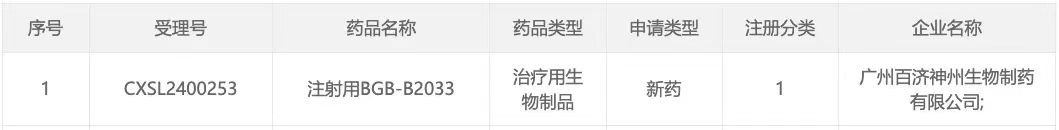
来自:CDE 官网
BGB-B2033 推测是一款双特异性抗体。去年 8 月,百济首款自主研发的双特异性抗体 CEA/4-1BB 双抗 BGB-B167 已进入临床阶段,正在美国、澳大利亚开展 I 期临床试验(登记号:NCT05494762),今年 1 月已完成全部受试者的招募工作。
百济此前披露,在肿瘤领域重点布局了两款双抗且计划均于本年度进入临床阶段,这两款双抗分别靶向 Claudin6/CD3 以及 MUC1/CD16。此次申报的 BGB-B2033 大概率是其中之一。
2023 年百济神州核心自研药物迎来重要进展。BTK 抑制剂百悦泽®(泽布替尼)全球销售额达 13 亿美元,成为国内首个「十亿美元分子」。目前,百济神州在研药物管线超过 50 款,覆盖多种技术平台和药物模式,包括单抗、双抗/多抗、ADC、细胞治疗、mRNA 等。
据财报,百济神州预计将于 2024 年,启动至少 10 个新分子实体的首次人体临床试验,加速下一阶段的研发浪潮。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..