Elicio Therapeutics公司今日宣布,其在研疗法ELI-002 7P作为携带KRAS突变的胰腺导管腺癌(PDAC)辅助治疗的2期临床试验AMPLIFY-7P已经完成首位患者给药。ELI-002 7P是一种创新的在研抗癌疫苗,采用Elicio的淋巴结靶向两亲性(AMP)技术开发,旨在治疗由七种常见KRAS突变(G12D、G12R、G12V、G12A、G12C、G12S、G13D)驱动的癌症。
最近发表在Nature Medicine上的1期临床试验数据突显了ELI-002的潜力:
这项研究涉及25名实体瘤患者(20名胰腺癌,5名结直肠癌),这些患者在局部区域治疗后发现存在KRAS突变阳性最小残余疾病。他们接受了包含两种KRAS突变体多肽的ELI-002 2P的治疗。研究结果显示:
84%的患者(21/25)观察到KRAS突变体特异性T细胞应答,其中59%表现出CD4阳性和CD8阳性T细胞应答。
84%的患者(21/25)观察到肿瘤生物标志物应答,6/25患者(24%;3名胰腺癌,3名结直肠癌)实现生物标志物清除。
在中位随访8.5个月后,这25名患者的中位无复发生存期(RFS)为16.33个月。
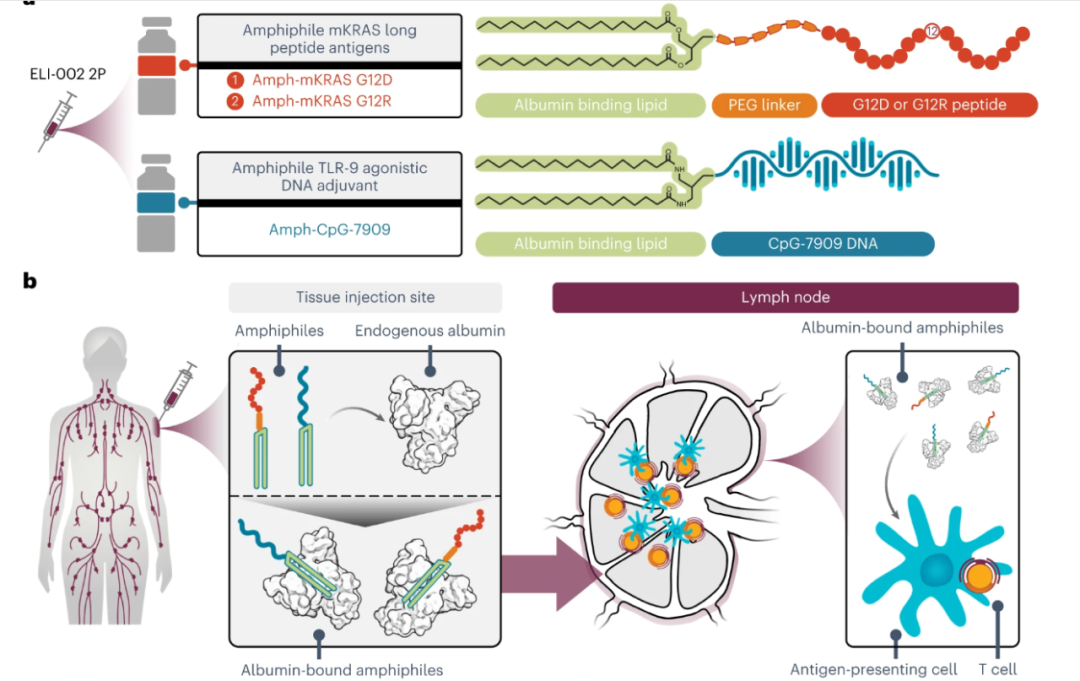
▲ELI-002的作用机制(图片来源:参考资料[3])
这一研究同时发现ELI-002 2P的疗效与T细胞应答具有相关性:
在T细胞应答水平高于中位数值的患者中,中位RFS尚未达到,而在低于中位数值的患者中为4.01个月(HR=0.14,95% CI,0.03-0.63,p=0.0167)。
T细胞应答高于中位数值的患者的疾病进展或死亡风险降低了86%。
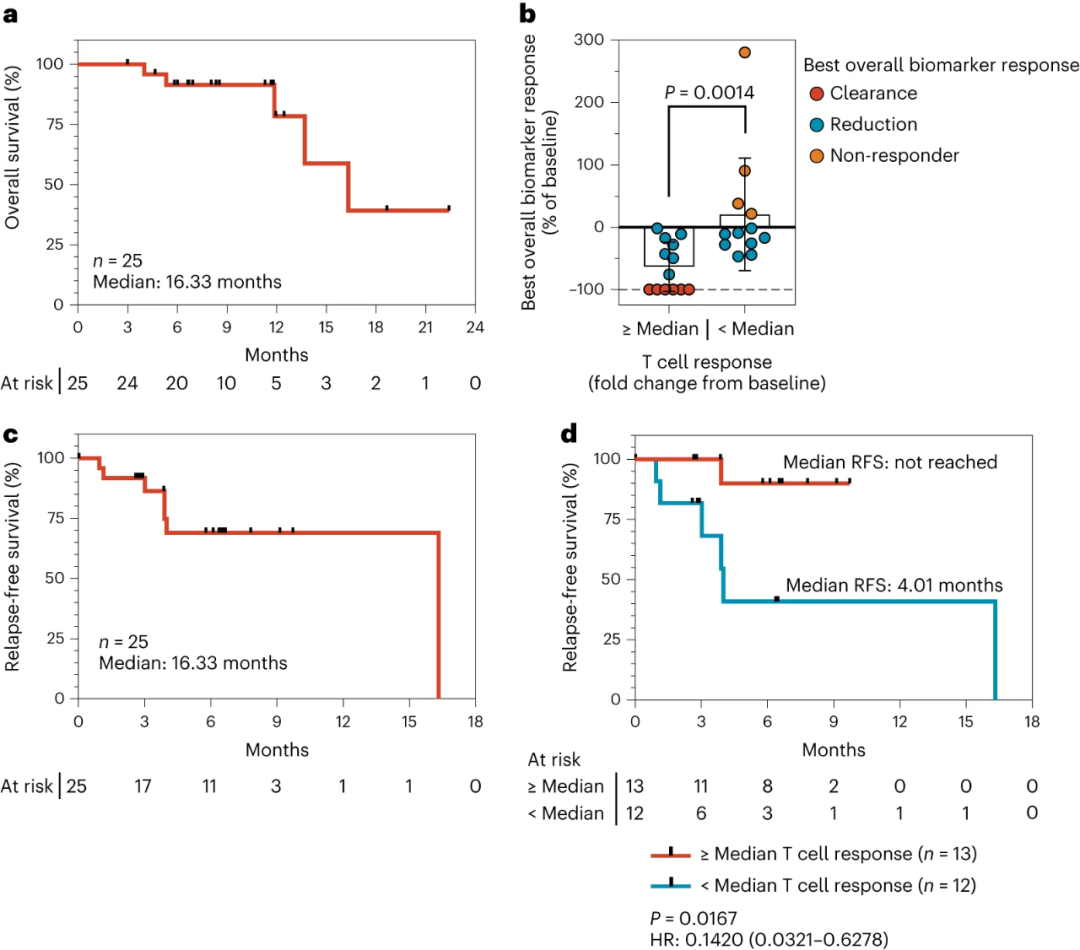
▲ELI-002 2P的疗效与T细胞应答水平具有相关性(图片来源:参考资料[3])
ELI-002 2P的安全性良好,未发现安全问题,未观察到剂量限制性毒性和≥3级治疗相关不良事件。
KRAS突变是人类癌症中最普遍的突变之一。ELI-002 7P配方针对的七种KRAS突变存在于四分之一的所有实体瘤中。具体来说93%的PDAC和52%的结直肠癌均包含KRAS突变。此外,27%的非小细胞肺癌包含KRAS突变。与其他针对KRAS的治疗方法(特别是小分子KRAS抑制剂)相比,ELI-002 7P疫苗的靶向范围更广,可能改善对患者的覆盖范围并延长疗效,因为它们更不容易受到耐药突变的限制。
参考资料:
[1] Elicio Therapeutics Announces First Patient Dosed in Randomized Phase 2 Pancreatic Cancer Study. Retrieved January 11, 2024, from https://elicio.com/press_releases/elicio-therapeutics-announces-first-patient-dosed-in-randomized-phase-2-pancreatic-cancer-study/
[2] Nature Medicine Publishes Updated Preliminary Phase 1 Data From Elicio Therapeutic’s AMPLIFY-201 Phase 1 Solid Tumor Study of ELI-002. Retrieved January 11, 2024, from https://elicio.com/press_releases/nature-medicine-publishes-updated-preliminary-phase-1-data-from-elicio-therapeutics-amplify-201-phase-1-solid-tumor-study-of-eli-002/
[3] Pant et al., (2024). Lymph-node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: the phase 1 AMPLIFY-201 trial. Nature Medicine, https://doi.org/10.1038/s41591-023-02760-3
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..