12 月 26 日,据 CDE 药物临床试验登记与信息公示平台显示,信达生物启动了 GLP-1R/GCGR 激动剂玛仕度肽(IBI362)头对头司美格鲁肽 III 期临床试验(登记号:CTR20234187)。
该研究旨在评估 IBI362 较司美格鲁肽在经单纯饮食运动干预伴/不伴二甲双胍单药治疗血糖、体重控制不佳的中国早期 2 型糖尿病合并肥胖受试者中的疗效和安全性。主要终点为第 40 周糖化血红蛋白(HbA1c)<7.0% 且体重较基线下降 ≥ 10% 的患者比例。
试验纳入标准

来自:CDE 官网
今年 10 月,信达公布的 9 mg 玛仕度肽治疗肥胖的 48 周 II 期研究数据结果显示:玛仕度肽 9 mg 48 周相较安慰剂体重降幅达 18.6%,体重下降超过 15%/20% 的受试者比例相较 24 周显著增加。
具体来看:
疗效方面,中重度肥胖受试者达成快速且强效的减重,减重效果媲美代谢手术:
2023 年 5 月,该研究主要终点达成,治疗 24 周后,玛仕度肽 9 mg 组体重较基线的平均百分比变化与安慰剂组的治疗差值达−15.4%,分别有 31.7% 和 21.7% 的受试者体重较基线下降至少 15% 和 20%。
在达到 24 周主要终点后,59 例受试者(玛仕度肽组 43/60 例,安慰剂组 16/20 例;整体平均基线 BMI 34.7 kg/m2,平均基线体重 98.4 kg)同意继续接受 24 周研究药物双盲延长期治疗。
治疗 48 周后,玛仕度肽 9 mg 组体重较基线的平均百分比变化与安慰剂组的治疗差值达−18.6%,平均变化值与安慰剂组的差值达−17.8 kg;玛仕度肽 9 mg 组中 51.2% 的受试者体重较基线下降 15% 以上,34.9% 的受试者体重较基线下降 20% 以上。
与体重变化相对应,48 周治疗期间玛仕度肽 9 mg 组受试者的腰围和血压等指标持续下降。
此外,多重代谢获益,肝脏脂肪含量大比例下降:
在基线肝脏脂肪含量(由 MRI-PDFF 测量)超过 5%# 的受试者中,玛仕度肽 9 mg 组治疗 24 周后肝脏脂肪含量较基线平均百分比下降 73.3%。在所有玛仕度肽 9 mg 组受试者中,丙氨酸氨基转移酶(ALT)水平在治疗 24 周后相对安慰剂的降幅达 45.5%。以上获益在至 48 周延长治疗期继续维持。# 美国肝病研究学会 NAFLD 指南推荐以 MRI-PDFF 测量的肝脏脂肪含量 5% 作为脂肪肝诊断切点。
在 24 周主要终点时,玛仕度肽 9 mg 组甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)和血尿酸水平(UA)下降幅度显著优于安慰剂,且降幅在至 48 周延长治疗期继续维持;高密度脂蛋白胆固醇(HDL-C)水平在整个 48 周治疗期间维持稳定。
在安全性方面,高剂量安全性和耐受性优异,无受试者因不良事件终止治疗。
玛仕度肽是信达与礼来共同开发的新药,协议于 2019 年 8 月签订。当前,该药已经在 2 型糖尿病和肥胖症领域双线布局,均推进到 3 期临床;还获批临床用于 NASH,即将对 NASH 启动相应研究。
玛仕度肽 III 期临床试验4
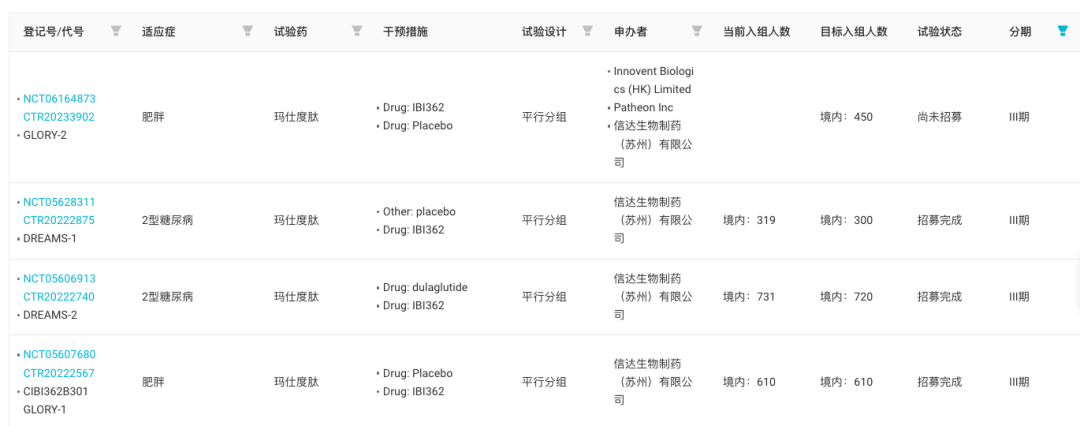
来自:Insight 数据库网页版
信达此前表示,预计在 2023 年末至 2024 年初就将提交玛仕度肽上市申请。在新一代 GLP-1 类药物被广泛认为是修美乐、K 药之后的下一代药王,甚至潜在峰值销售额预估将超越前几任的当下,玛仕度肽在中国的上市也将为信达提供 PD-1 信迪利单抗之后第二个业绩腾飞点,支撑信达完成未来 4-5 年实现 200 亿量级营收的目标。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..