1、Xilio Therapeutics登陆纳斯达克,推进肿瘤选择性免疫疗法研发
今日,Xilio Therapeutics(以下简称“Xilio”)宣布正式登陆纳斯达克,计划通过IPO募集约1.176亿美元。Xilio是一家致力于为癌症患者开发强效、肿瘤选择性免疫疗法的生物技术公司,今年2月该公司完成9500万美元的C轮融资,武田(Takeda)等参投。
Xilio成立于2016年,总部位于马萨诸塞州沃尔瑟姆,专注于利用免疫系统实现深度、持久的临床反应,以改善癌症患者的生活。Xilio利用其专有的“地理精确解决方案”(geographically precise solutions,GPS)平台,改造强效癌症免疫疗法,使其在肿瘤部位选择性地释放免疫系统的力量,将疗效最大化,同时降低与某些免疫肿瘤学疗法相关的显著毒性。目前,该公司已建立了基于GPS平台的一系列细胞因子和检查点抑制剂候选产品管线,包括XTX101(肿瘤选择性抗CTLA-4单克隆抗体)、XTX202(肿瘤选择性IL-2)、XTX301(肿瘤选择性IL-12)、XTX401(肿瘤选择性IL-15)。
根据招股章程,Xilio此次IPO所得款项净额,拟用于以下用途:
约3000万至3500万美元用于XTX202临床开发,包括进行治疗实体瘤患者的1/2期临床试验;
约2000万至2500万美元用于XTX301临床开发,包括新药临床试验(IND)支持性研究和IND递交,以及1期临床试验的开展;
约1000万至1500万美元用于XTX101临床开发,包括完成剂量递增1期临床试验,以及开展2期临床试验;
其余部分用于推进其他肿瘤选择性细胞因子项目研发,以及用于营运资金和其他一般企业用途。
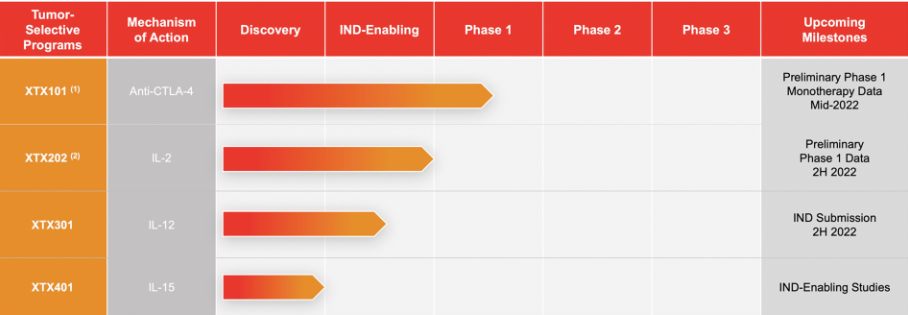
▲Xilio的在研管线(图片来源:Xilio招股书)
据招股章程介绍,XTX101是一种在研肿瘤选择性抗CTLA-4单克隆抗体,旨在将抗CTLA-4效应精准地限制在肿瘤内部,防止产生肿瘤外的外周效应。这一策略可能改善治疗指数(therapeutic index),克服其他抗CTLA-4抗体在效力和耐受性上受到的限制。在临床前研究中,XTX101耐受性良好,并实现了强力的肿瘤生长抑制,包括通过肿瘤选择性免疫激活达到完全缓解。目前,该药物单药治疗晚期实体瘤患者的1/2期临床试验已于近日启动。今年5月,Xilio与默沙东(MSD)达成临床试验合作协议,评估XTX101与默沙东的抗PD-1疗法Keytruda联用,治疗实体瘤患者的安全性和疗效。
XTX202是一种在研肿瘤选择性IL-2。在临床前研究中,观察到XTX202以蛋白酶依赖性方式被激活,表现出肿瘤生长抑制作用,并且在达10 mg/kg的非人灵长类动物模型(NHP)中具有良好的耐受性。今年10月,美国FDA批准了XTX202的IND申请,该药物用于多种实体瘤的1/2期试验预计将在2022年第一季度启动。
此外,基于GPS平台,Xilio还开发了在研肿瘤选择性IL-12 XTX301,计划于2022年下半年递交IND申请。另外,该公司的在研肿瘤选择性IL-15 XTX401也正在进行临床前研究。在临床前模型中,这两种细胞因子候选产品均表现出具有最小外周效应的肿瘤选择性活性,在小鼠模型中显示出肿瘤生长抑制作用,并且在NHP模型的多剂量研究中具有良好的耐受性。
2、Ventyx Biosciences登陆纳斯达克,推进炎症性疾病和自身免疫性疾病新药研发
Ventyx Biosciences(以下简称“Ventyx”)宣布于10月21日正式登陆纳斯达克,计划通过IPO募集约1.515亿美元。值得一提的是,Ventyx于今年3月宣布完成1.14亿美元融资,并走出隐匿模式。上月又完成一笔5100万美元B轮融资,奥博资本(OrbiMed)、Vivo Capital(维梧资本)、启明创投(Qiming Venture)等参投。
Ventyx是一家临床阶段的生物技术公司,总部位于加利福尼亚州,专注于为数百万患有炎症性疾病和自身免疫性疾病的患者开发新疗法。Ventyx合并了三家公司的在研产品,包括Oppilan Pharma靶向鞘氨醇-1-磷酸受体1(S1P1R)的在研产品,Zomagen Biosciences靶向NLRP3炎症小体的在研产品,以及原Ventyx Biosciences靶向酪氨酸激酶2(TYK2)的在研产品。目前,Ventyx已建立由4个专注于炎症性疾病和自身免疫性疾病的候选药物组成的管线,包括2种处于临床阶段的候选药物。这些产品主要为小分子候选药物,拟开发用于银屑病、炎症性肠病(IBD)、心血管疾病和风湿病等。
根据招股章程,Ventyx此次IPO所得款项净额,拟用于以下用途:
约7500万至8500万美元用于VTX958临床开发,包括完成针对银屑病和其他适应症的2期临床试验;
约4500万至5500万美元用于VTX002临床开发,包括完成针对溃疡性结肠炎(UC)的2期临床试验;
约500万至1100万美元用于VTX2735临床开发,包括完成针对健康志愿者的单剂量和多剂量递增(SAD/MAD)1期临床试验;
约1000万至2000万美元用于公司其他开发项目的研究活动和临床前开发,包括中枢神经渗透性NLRP3抑制剂项目的新药临床试验(IND)申请;
若有剩余部分,用于业务发展活动、营运资金和其他一般企业用途。
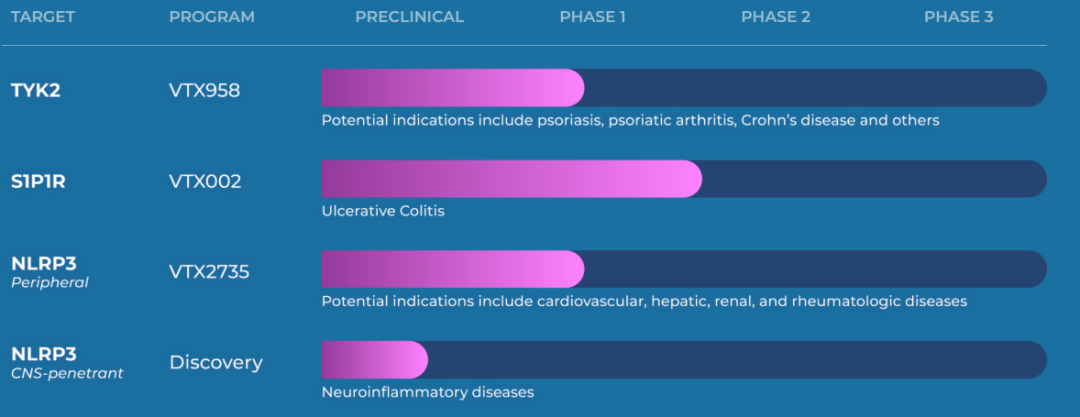
▲Ventyx的在研管线(图片来源:Ventyx官网)
Ventyx的先导候选药物VTX958是一种在研口服、选择性TYK2抑制剂,拟开发适应症为广泛的免疫介导疾病,如银屑病、炎症性肠病(IBD)、银屑病关节炎和狼疮。目前,该药物的1期临床试验的单剂量递增部分已经完成,预计于2021年第四季度启动本试验的MAD部分。TYK2是JAK家族中的一种细胞内信号激酶,而JAK信号转导和转录激活子(STAT)信号通路与许多炎症和自身免疫性疾病的发病机制有关。通过抑制TYK2介导的信号转导,VTX958有可能抑制慢性炎症,同时避免抑制JAK家族的其他相关成员,从而降低感染和其他副作用的相关风险。
VTX002是一种在研口服、选择性S1P1R调节剂,拟用于治疗溃疡性结肠炎(UC)。目前,该药物用于健康志愿者的1期临床试验已经完成,试验结果显示,VTX002在所有试验剂量下均耐受良好,未发生严重不良事件。此外,VTX002显示淋巴细胞绝对计数(ALC)减少,而ALC是S1P1介导疾病的公认生物标志物。基于此,VTX002的随机、安慰剂对照2期临床试验预计将于2021年第四季度启动,将该药物拓展用于其他相关免疫学适应症的临床试验也可能进一步开展。
VTX2735是一种在研口服、选择性和外周限制性(不通过血脑屏障)NLRP3抑制剂,拟开发用于治疗全身性炎症性疾病,如心血管、肝脏、肾脏和风湿病。该药物已于2021年9月获美国FDA的IND批准,并计划在2021年第四季度启动针对健康志愿者的1期临床试验。该药物已在细胞试验中证明了NLRP3抑制作用,在动物模型中具有体内药效学活性,并且在多个临床前物种中具有高口服生物利用度。招股书显示,除了VTX2735,Ventyx还在开发NLRP3抑制剂的产品组合,拟用于NLRP3炎症小体激活驱动的多种适应症。该公司的NLRP3抑制剂产品组合还包括中枢神经渗透性(CNS-penetrant)抑制剂,被认为对阿尔茨海默病、帕金森病、肌萎缩侧索硬化和多发性硬化(MS)具有潜在的治疗效用。
参考阅读:前沿 | 《自然》: 炎症促发阿尔茨海默病再添力证,炎性小体激活引发tau蛋白异常
参考资料:
[1]Xilio Therapeutics Announces Pricing of Initial Public Offering. Retrieved 2021-10-23, from https://www.businesswire.com/news/home/20211021006123/en
[2]Xilio Therapeutics的在研管线. Retrieved 2021-10-23, from https://www.sec.gov/Archives/edgar/data/1840233/000110465921128952/tm2115750-18_424b4.htm
[3]Ventyx Biosciences Announces Pricing of Upsized Initial Public Offering. Retrieved 2021-10-21, from https://www.globenewswire.com/news-release/2021/10/21/2317909/0/en/Ventyx-Biosciences-Announces-Pricing-of-Upsized-Initial-Public-Offering.html
[4]Ventyx的在研管线. Retrieved 2021-10-22, from https://ventyxbio.com/pipeline/
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..