6月30日,艾力斯宣布拟与 ArriVent Biopharma 签署《全球技术转让和授权协议》和《普通股认购协议》,就伏美替尼在海外市场的开发及商业化达成整体合作。
艾力斯拟授权 ArriVent 使用公司伏美替尼相关专利和专有技术,在除中国大 陆、台湾、香港和澳门外的地区独家开发(包括研发、生产、进口、出口、使用、 销售等)伏美替尼的权利,可获得 4000 万美元的首付款,累计不超过 7.65 亿美元的研发和销售里程碑款项(达到约定的研发或销售里程碑事件),销售提成费,以及 ArriVent 一定比例的股份,ArriVent 将成为公司的参股公司。
伏美替尼是高选择性、不可逆第三代表皮生长因子受体酪氨酸激酶抑制剂 (EGFR-TKI),为公司自主研发的 1 类小分子靶向药,表现出了良好的疗效及安 全性,目前已获批用于 EGFR 突变非小细胞肺癌患者的二线治疗,具有“双活性、 5 高选择、强缩瘤、安全佳”的特点。
根据发表在《柳叶刀·呼吸医学》的 IIb 期临床数据显示,患者的客观缓解率(ORR)达 74%,中位无进展生存期(mPFS)达 9.6 个月,疾病控制率(DCR) 达 94%;特别针对脑转移患者,在 WCLC 2020 会议中披露的数据显示,在 IIa 期 剂量扩展研究的 160mg 亚组中,伏美替尼的 CNS(中枢神经系统)ORR 达到 84.6%,CNS mPFS 达 19.3 个月,CNS DCR 达 100%,显示出了伏美替尼的差异化优势。
伏美替尼的二线治疗适应证(即针对既往经表皮生长因子受体酪氨酸激酶抑 制剂治疗时或治疗后出现疾病进展、并且经检测确认存在 EGFR T790M 突变阳 性的局部晚期或转移性 NSCLC 成人患者的治疗)已于 2021 年 3 月 3 日由国家 药品监督管理局获批在国内上市;一线治疗适应证(即针对具有 EGFR 外显子 19 缺失或外显子 21(L858R)置换突变的局部晚期或转移性非小细胞肺癌成人患者 的治疗)的 III 期临床试验已于 2019 年底在国内完成患者入组,预计将于 2021 年申报 NDA;辅助治疗适应证(针对接受根治性切除伴或不伴辅助化疗后的表 皮生长因子受体(EGFR)突变阳性 II-IIIA 期非小细胞肺癌患者的治疗)已于 2021 年 1 月在国内获批 IND,目前处于 III 期临床试验阶段;针对 20 外显子插入突变 适应证(即针对 EGFR 20 外显子插入突变的局部晚期或转移性非小细胞肺癌成 人患者的治疗)目前已在国内开展 Ib 期临床研究。
ArriVent 成立于 2021 年 4 月,目前已完成首轮融资,募集了数千万美元的资金。
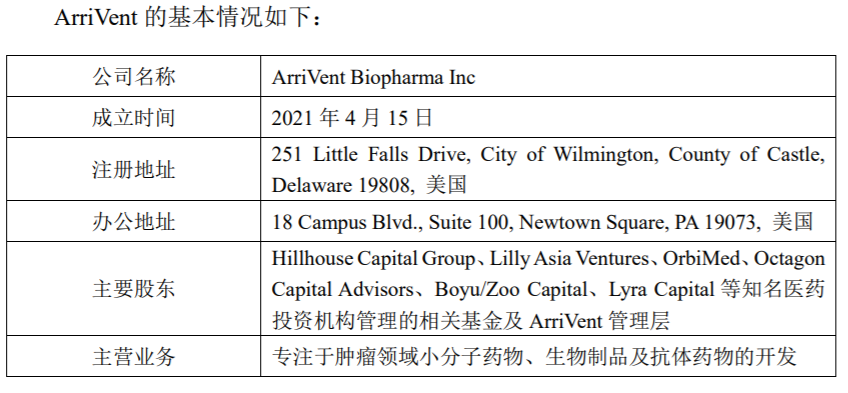
ArriVent 的董事长兼首席执行官为 Zhengbin (Bing) Yao 博士,其在制药行业 具有广泛的研发及管理经验。他曾于 2018 年联合创立了 Viela Bio 公司,并担任 该公司的董事长及首席执行官,Viela Bio(VIE.O)公司曾在美国纳斯达克上市, 并于 2021 年被 Horizon Therapeutics 以约 30.5 亿美元的价格收购。此前,他曾在 基因泰克、Tanox、阿斯利康等知名药企担任研发及管理职务,并在呼吸、炎症 及免疫肿瘤创新药物的研发领域具有丰富的经验。目前 ArriVent 已完成关键研发 和管理团队的组建,相关人员具有海外知名药企的管理及研发经验,具备推进创 新药物在海外注册上市的能力。
PS:医药项目交易是新形势下中国企业的重要经营活动,医药魔方NextPharma数据医药交易模块“追踪交易动态,把握创新风向”。您只需关注医药魔方plus,订阅“医药交易”,即可接收日常重要交易资讯预警,不会错过重要行业动向。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..