今日,欧洲药品管理局(EMA)的人用药品委员会(CHMP)宣布,启动对科兴中维开发的新冠灭活疫苗克尔来福的滚动审评(rolling review)。滚动审评是EMA在公共健康危机时期用于加快药品评估的一种方式,有利于更为快速的完成审评过程。
克尔来福是一款新冠灭活疫苗,同时加入了氢氧化铝作为提高疫苗效力的佐剂(adjuvant)。它已经在世界上32个国家和行政区获得批准,用于在18岁以上的成年人中预防COVID-19,已经有超过2.6亿疫苗被分发到中国和世界各地。
世界卫生组织目前正在评估是否将克尔来福纳入紧急使用名单(emergency use list, EUL)。列入EUL将促进它在全球各个国家的批准流程,加快疫苗进口和使用的速度,并且让世界卫生组织可以通过名为COVAX的疫苗购买和分发渠道,向世界各国,尤其是中低收入国家分发疫苗。
世界卫生组织的审评文件中支持克尔来福的临床试验数据包括在土耳其、印度尼西亚、巴西进行的随机对照3期临床试验,以及在智利进行的真实世界数据分析和在巴西进行的针对P.1新冠突变病毒的防护效力研究。克尔来福防护COVID-19的效力在50%到84%之间,防护因为COVID-19住院的效力在85%到100%之间。点击文末“阅读全文/Read more”即可下载世界卫生组织审评文件。
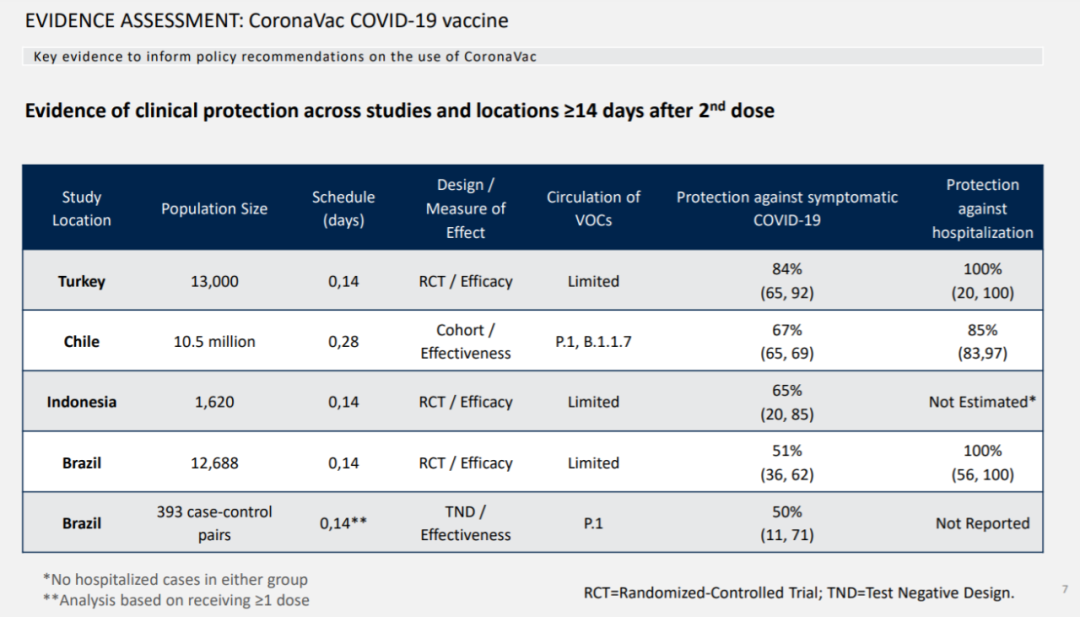
▲接种两剂CoronaVac疫苗14天后的保护效力数据(图片来源:WHO官网)
EMA表示,人用药品委员会决定启动滚动审评是基于非临床实验研究和临床试验的初步结果。这些研究显示,克尔来福能够激发针对新冠病毒的中和抗体的产生,可帮助预防COVID-19。如果获得EMA的批准,克尔来福将能够在欧盟27个国家中使用。
参考资料:
[1] EMA starts rolling review of COVID-19 Vaccine (VeroCell) Inactivated. Retrieved May 4, 2021, from https://www.ema.europa.eu/en/news/ema-starts-rolling-review-covid-19-vaccine-vero-cell-inactivated
[2] Evidence Assessment: Sinovac/CoronaVac COVID-19 vaccine.Retrieved May 4, 2021, from https://cdn.who.int/media/docs/default-source/immunization/sage/2021/april/5_sage29apr2021_critical-evidence_sinovac.pdf?sfvrsn=2488098d_5
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..