
2月26日,福建省医保局公布了《福建省药品集中带量采购文件》的通知。此前在1月14日,福建医保局发布了该文件的征求意见稿,今日发布的正式版文件中则明确了关于接下来关于申报材料、模拟报价、正式报价等各项任务的时间。在医保相关政策探索方面福建一直走在前面,此次通过福建对于未过一致性评价品种的集采规定,一定程度上也能感知到地方集采试点的相关趋势。
福建省医保局正式公布了此次集采的14个采购品种及相应采购量。14个采购品种是在采购金额较大、竞争充分、临床使用成熟、同一通用名尚未有通一致性评价的药品中通过专家遴选形式而确定,采购基础量则是按照福建全省公立医疗机构2018年7月1日至2019年6月30日同通用名仿制药(不含参比制剂、通过 FDA 认证且在欧美有销售的仿制药)总用量的70%来确定。
采购品种及约定采购量
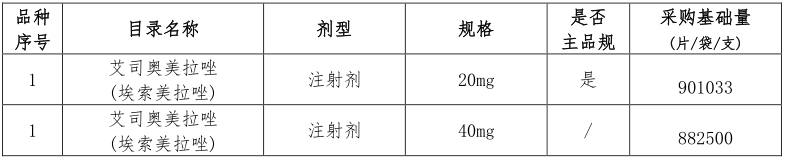

注:(1)口服常释剂型:普通片剂(片剂、肠溶片、包衣片、薄膜衣片、糖衣片、浸膏片、
分散片、划痕片)、硬胶囊、软胶囊(胶丸)、肠溶胶囊;不包括口腔崩解片(口崩片);
(2)注射剂:注射剂、注射液、注射用溶液剂、静脉滴注用注射液、注射用混悬液、注射液无菌粉末、静脉注射针剂、水针、注射用乳剂、粉针剂、针剂、无菌粉针、冻干粉针。
01 时间紧、规则新
福建省此次集采政策在以下层面值得重视。
首先是更紧张的操作时间。
申报材料网上填报从明日即开始进行持续时间为一周(2月27日~3月4日),这也意味着扣除周末仅有5个工作日。公示的时间同样为5个工作日,3月18日为第一轮申报报价时间,当天完成开标解密;当天晚7时到次日下午5时则为第二轮议价谈判确认时间,当天公布中选结果。
值得注意的是,当前还有相当多企业处于远程办公的状态,同时也应该是出于疫情考虑,相较于征求意见版,此次将申报方式由线下的纸质版申报改为了网上申报。在征求意见稿中,要求相关企业申报采取网上申报的方式,企业报价则通过企业授权代理人通过纸质报价函对申报药品进行现场报价。而正式版调整为,数字证书是企业网上申报的唯一标识,申报企业凭数字证书登录平台进行网上药品申报、资料提交、信息澄清、报价等相关操作。
其次,是更为严格的降价规则。
相较于国家集采,福建省集采设置了新的中选规则,共分为两个步骤,第一个步骤是预中选品种确定,第二个步骤是拟中选品种确定。有行业人士向E药经理人表示,此举更多的是为了避免一些独家品种降幅不够,甚至“坐地起价”的情况。对于独家品种来说,具体是否能够入围仍然要看降幅。
还有值得注意的是,正式版再次强调了含量差价比的规则。
申报报价中第四点明确,“以申报价作为基数按现行药品含量差比价规则计算确定的申报产品包装价,不应高于按含量差比价规则折算后的同品种竞争组现行最高销售限价,且原则上不应高于本企业同品种2019 年全国最低省级集中采购价。”而显然,对于企业来说这并不算是个好消息。
高门槛竞争
福建自正式执行集中带量采购起采购周期为 1 年,期内若提前完成当年约定采购量,超过部分中选企业仍按中选价进行供应,直至采购周期届满。
采购主体除了全省公立医疗机构,还鼓励在闽部队、武警医疗机构及其他医疗机构参加药品集中带量采购活动。
在集中带量采购结果执行周期中,各公立医疗机构将优先使用集中带量采购中选品种,并确保完成采购基础量,中选药品使用量原则上不少于同一通用名仿制药品使用总量的60%。
总的来看,拼价格、拼质量、拼产能,是此次竞赛的关键,从福建医保局制定的入选规则来看足够见此次福建集采的门槛之高。
入选企业要具备一定规模,并且能够保证质量和产能。
根据申报资质要求,申报企业需要属 2018 年《中国医药统计年报(综合册)》中“工业企业法人单位按医药工业主营业务收入排序”前500家的企业(含集团所属企业),或是下表涉及企业。在产能方面更是明确要求,申报品种全年产能达到本次采购数量2倍(含)以上。在质量门槛上,福建设置的申报企业资质要求明确,挂网文件正式公布日的前两年内申报品种不存在被相关药监部门检测不合格或处罚并公告的情况,前五年内申报企业在GMP认证中无不予通过的情况等。
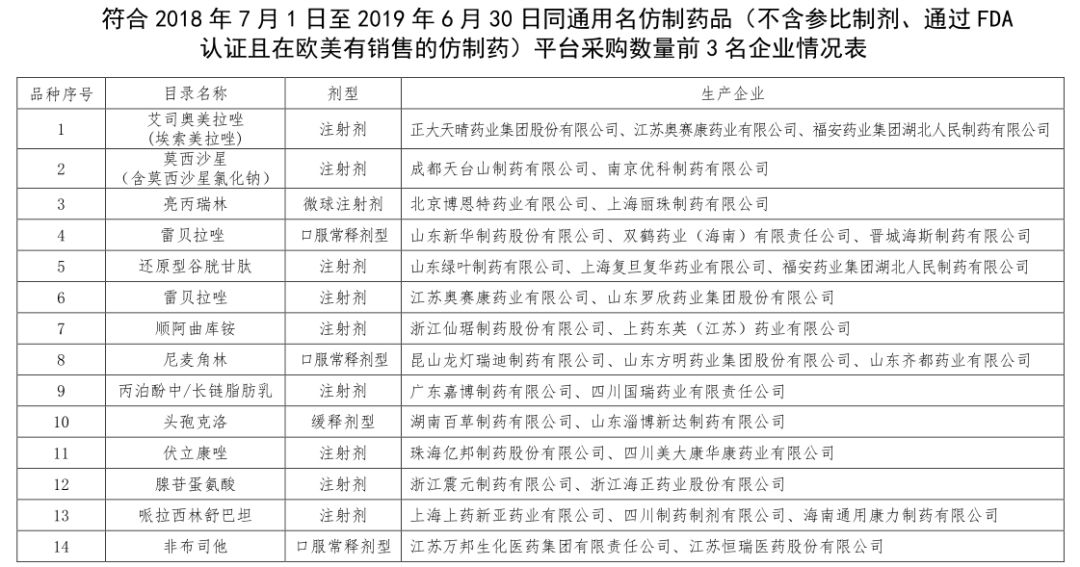
值得注意的是,以上图表中的企业几乎大部分是本土药企,只有昆山龙灯瑞迪制药有限公司除外。此前瑞迪制药的奥氮平片成功入选国家集采,此次其参与的报价策略值得关注。
正式版文件还在申报要求中指出,“鼓励原研药品、参比制剂、通过 FDA 认证药品的企业参与申报,但不区分质量层次”,这也就意味着,对于本土药企来说竞争面将扩大,而对于跨国药企来说价格策略的制定很重要。
而对于福建已挂网且符合申报条件的企业,无论参与此次集采与否都将面对纠结,要求表示,这类企业如未报名参加福建集中带量采购,将对相关企业涉及产品予以撤销挂网处理。而在此前征求意见稿中,对于该情形的具体要求是“将对相关涉及产品进行重点监控,如发现存在销售、使用异常等情形,根据具体情况处以约谈、通报批评、暂停挂网直至撤销挂网等处理”,正式版则是直接以撤销挂网处理,不留空间。
而参与企业中选需要闯过预中选和拟中选两大关。中选后的药品在履行合同中如有全国其他省级集中带量采购价格低于中选价格的,价格相应联动。并且严禁二次议价等类似情形,文件内容明确,“在购销合同签订后,医疗机构与中选企业不得再订立背离合同实质性内容的其他协议或提出除合同之外的任何利益性要求”。
从中选规则来看,价格之外,质量也尤为重要。
首先预中选品种确定准则上,同品种通过资质审核的企业数量≥2 家、最低报价只有1家企业的,则该企业的申报品种获得预中选资格。若仅有 1 家企业通过资质审核的,直接获得预中选资格。
当最低报价相同时,按以下原则依次处置:(1)2018年7月1日~2019年6月30日期间同品种福建省采购量大的企业的申报品种优先获得预中选资格,不同规格产品采购量合并计算;(2)如果申报企业产品均为福建未挂网产品,按照“工业企业法人单位按医药工业主营业务收入排序”排名靠前的企业申报品种优先获得预中选资格。
这是第一关,接下来是第二关。按照拟中选品种的确定准则,获得预中选资格的企业及申报品种,统一进入议价谈判确认程序。
1、通过资质审核企业数≥3 家的品种:预中选品种申报价格符合本次报价的有关要求,经双方确认后,获得拟中选资格。
2、通过资质审核企业数≤2 家的品种:①预中选品种申报价格降幅从高到低在所有预中选品种中排名前 50%(遇无法整除保留整数位)的,经双方确认后获得拟中选资格;②其余预中选品种:参考通过资质审核企业数≥3 家的拟中选品种平均降幅的一定比例确定议价谈判最低降幅。申报价格符合降幅要求且达成一致意见的,即可获得拟中选资格。若不参加或不接受议价谈判的,该品种作流标处理,省药械联合采购中心对相关产品实施重点监测,按月公布各医疗机构采购量,并列入医保稽核监管必查项目。
03 参与者警戒线
福建在此次采购试点更是对于违规行为做出相当详细的规定,参与企业应提高重视程度,且其他地区试点有可能进行参考。
文件明确,申报企业、配送企业如有以下行为,经有关部门认定情节严重的将被列入“违规名单”。
1、提供处方回扣或其他商业贿赂,进行非法促销活动。
2、以低于成本的价格恶意申报,扰乱市场秩序。
3、相互串通申报,排斥其他申报企业的公平竞争,损害采购方或者其他申报企业的合法利益。
4、以向采购方、采购机构行贿等手段牟取中选。
5、提供虚假证明文件及文献资料,或者以其他方式弄虚作假,骗取中选。
6、未在规定期限内签订带量购销合同。
7、中选企业、配送企业未按采购方以及法律法规要求实行配送。
8、中选后放弃中选资格。
9、不履行供货承诺,影响到临床使用。
10、中选药品中选后发生严重质量问题。
11、中选药品中选后在规定的抽检或飞行检查中发现严重违背在申报材料中作出的承诺。
12、其他违反法律法规的行为。
列入“违规名单”的,按以下条款处理。
申报企业、配送企业列入“违规名单”的,取消相关企业本次药品集中带量采购的申报、中选、配送资格,并按照《福建省医疗保障管理委员会办公室关于印发福建省药品联合限价阳光采购药品供应履约管理办法的通知》有关规定处理。同时视情节轻重取消上述企业在列入“违规名单”之日起 2 年内参与福建省药品采购活动的资格。
患者使用中选药品时,因中选药品生产质量原因造成人身伤害的,按照《药品管理法》等法律法规,由中选企业承担全部赔偿责任。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..