全球四分之一的人曾感染过乙型肝炎病毒(HBV),现阶段约有2.5亿的慢性乙肝病毒感染者,这使他们面临进展性肝病,肝硬化,肝功能衰竭和肝细胞癌风险。在感染HBV的成年人中有 95%的可实现自发性清除病毒,而有90%的新生儿将会发展为慢性感染。
由于HBV感染不会诱导干扰素应答,因此HBV是一种与先天免疫系统相关的隐形病毒。因此,HBV清除取决于成功的适应性免疫应答。 实际上,多特异性和有活力的HBV特异性CD8 + T细胞反应与病毒清除有关,而HBV特异性CD8 + T细胞衰竭是持续感染的标志。
然而,较少关注靶向HBV包膜蛋白HBV表面抗原(HBsAg)的中和抗体的作用。事实上,乙型肝炎表面抗体(抗HBs)多数只在感染HBV的人群实现 HBsAg 消失后的血液中才可检测到(少数出现病毒变异的感染者可同时出现HBsAg和抗HBs),无论是在急性感染痊愈后,还是在罕见的自发性或药物诱导的慢性HBV感染清除的情况下。从上述的见解中可发现抗HBs在HBV清除中似乎没有起主要作用。
另一方面,抗HBs已被确立为诊断工具,在急性HBV感染痊愈后或疫苗接种后的保护性免疫以及慢性HBV感染的“功能性治愈”(HBsAg至抗HBs血清转换)后。
然而,有一些临床观察结果对抗HBs的这种次要作用进行了反驳。
首先,众所周知,乙型肝炎免疫球蛋白(HBIG)中含有的抗-HBs可防止感染母亲向新生儿的垂直传播以及先前HBV感染宿主中肝脏移植的再感染。
其次,用于肿瘤学和风湿病学的B细胞耗竭药物,例如抗CD20抗体利妥昔单抗,在HBV携带者中会诱导HBV再激活,甚至在实现“解决的”HBV患者中,其中细胞核HBV cccDNA 可作为病毒库持续数十年。
这些临床观察表明,抗HBs的作用比以前已获承认的更为突出。实际上,抗-HBs可阻断HBV细胞进入,阻断HBsAg的结合位点 —— 牛磺胆酸钠协同转运多肽(NTCP)受体,或通过结合参与相互作用的HBsAg的“抗原环”—— 硫酸乙酰肝素蛋白多糖(HSPG)在细胞进入的预先受体步骤中。
除了直接抑制细胞进入外,抗-HBs还介导内吞作用和随后的病毒粒子中和以及Fc介导的吞噬作用和杀死感染细胞。 此外,抗HBs,HBsAg和其他构成免疫复合物的成分可激活HBV特异性T细胞。
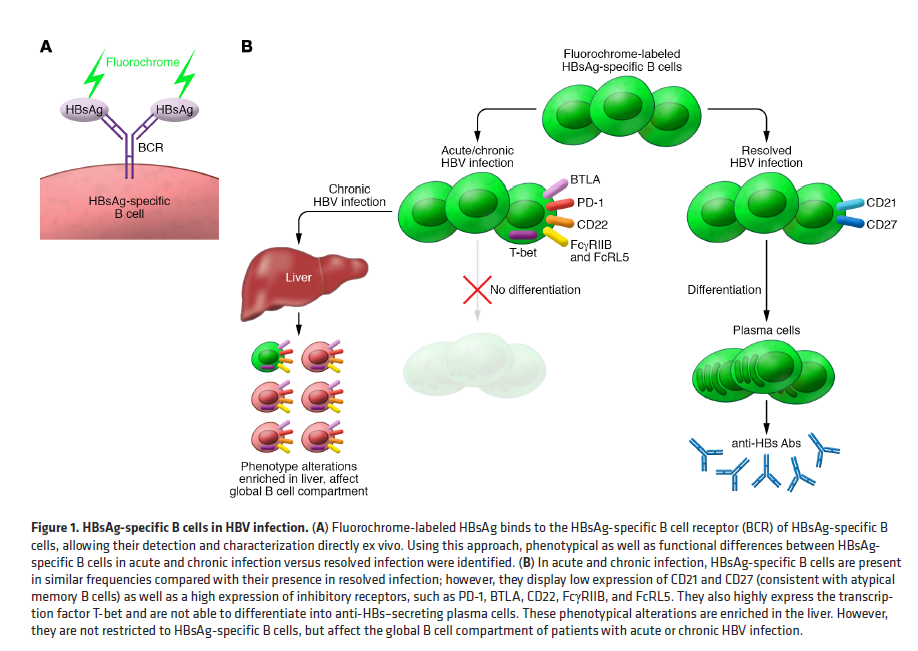
HBsAg特异性B细胞在急性和慢性HBV感染
鉴于抗HBs的这些重要的抗病毒功能,HBV免疫生物学中的一个主要开放问题是在急性和慢性HBV感染中HBsAg消失之前为何缺乏可检测的抗HBs。迄今为止,已经提出了关于缺乏抗HBs的两种似乎合理的假设解释:
首先,有人提出抗HBs是由HBsAg特异性B细胞在急性和慢性HBV感染中产生的,但是由于大量含有HBsAg的循环亚病毒颗粒的数量超过了完整的病毒颗粒,其数量级超过了一个数量级。
这一假设得到以下发现的支持:抗HBs与循环HBsAg的复合物当前的诊断分析尚无法识别,但在慢性感染患者中使用高灵敏度免疫分析可以检测到。
此外,早期和最近有关于HBsAg特异性B细胞功能障碍的报道,尤其是慢性HBV感染。实际上,从患有慢性HBV感染的患者中分离的B细胞显示出增殖能力降低并且在刺激后不能产生抗HBs。在慢性感染期间罕见的HBsAg消失事件后,这种功能缺陷获得恢复。
在近期的JCI杂志中, 来自 Bertoletti 实验室的Salimzadeh 和 Le Bert 等人和来自 Maini实验室的 Burton 等人通过利用新技术检测 HBsAgs 特异性B细胞,解决了急性和慢性HBV感染期间缺乏抗HBs的问题。
具体而言,他们利用荧光染料标记的重组HBsAg作为“诱饵”,通过离体FACS分析检测和表征HBsAg特异性B细胞。 引人注目的是,通过独立使用类似的方法,两组得出了相同的结果:
首先,HBsAg特异性B细胞以相似的频率存在于急性,慢性和解决的HBV感染中。
其次,从患有急性以及慢性(未解决的HBV感染)患者中分离的HBsAg特异性B细胞不能在体外成熟为抗HBs分泌细胞。
第三,在表型分析中,急性和慢性HBV感染中的这些HBsAg特异性B细胞类似于“非典型记忆B细胞”,其特征在于CD21和CD27的低表达,但是抑制性标记物如PD-1和转录因子T-bet却是高表达。
第四,Burton等人证明这些HBsAg特异性非典型记忆B细胞在肝脏,感染部位和HBV感染患者的炎症中积聚。
第五,这种表型和功能障碍不仅限于HBsAg特异性B细胞,还影响HBV感染患者的全身B细胞群,这一发现目前尚不明确,需要进一步研究证实。
第六,HBsAgs 特异性B细胞的功能可以通过特定的培养条件如PD-1阻断或添加IL-2,IL-21和CD40配体表达(CD40L-表达)饲养细胞中在体外部分恢复。
为乙型肝炎B细胞靶向研究打开了大门
这些结果清晰地证明B细胞功能障碍而非抗体耗竭是急性和慢性HBV感染中缺乏抗HBs的主要原因。因此,这些研究发现也为将B细胞作为新型抗病毒策略从而旨在实现功能性治愈(HBsAg血清学转化为抗HBs)慢乙肝的目标打开了大门。
事实上,目前开发的抗病毒策略,包括病毒进入抑制剂,病毒衣壳释放抑制剂,免疫调节剂或治疗性疫苗,都没有在大量患者中实现功能性治愈,即使与目前批准的抗病毒化合物如聚乙二醇化 IFN-α、核苷/核苷酸类似物(如替诺福韦或恩替卡韦)联合使用。
值得注意的是,Salimzadeh、Le Bert、Burton等人目前的研究。不是完成,而只是乙型肝炎领域B细胞靶向研究的开始,类似于近二十年前广泛引入肽/ MHC四聚体后新兴的T细胞研究。
实际上,仍然有许多悬而未决的问题,例如导致HBsAg特异性B细胞功能障碍的细胞和分子机制,例如,受损的滤泡辅助T(Tfh)细胞的参与及全身B细胞群的损伤机制和(临床)后果,以及在慢性HBV感染功能性治愈途径中恢复HBsA特异性B细胞功能的最佳策略是什么。
值得注意的是,PD-1阻断增强了猕猴体内对抗SIV的抗病毒B细胞免疫力。具体而言,确定用于恢复B细胞功能的最佳干预措施是非常重要的,例如,靶向单一还是多种抑制性受体或选择最有希望的细胞因子和饲养细胞用于体内和/或过继细胞转移等等。有了这些重要的问题和激动人心的机会,预计HBsAg特异性B细胞将成为未来几年的研究焦点。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..