5 月 12 日,CDE 官网显示,宝济药业注射用 KJ103 拟纳入优先审评,适用于高度致敏的肾移植患者进行脱敏治疗,有效清除预存 HLA 抗体预防超急性排斥反应。
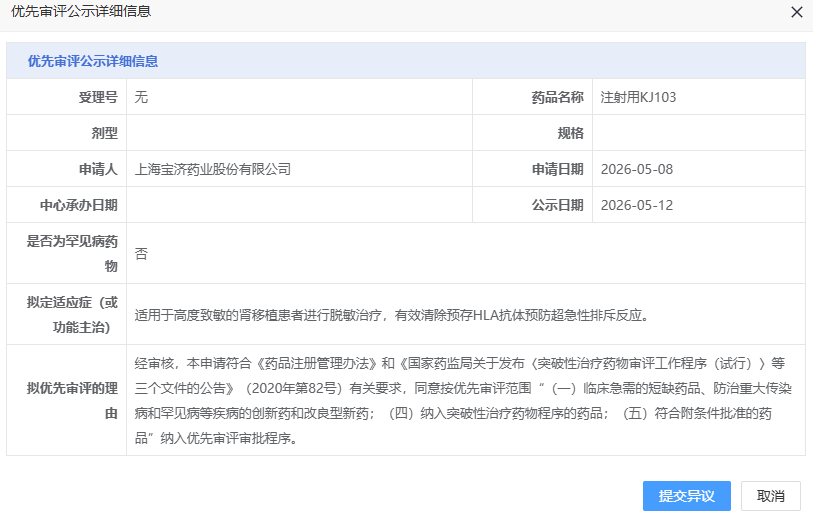
截图来源:CDE 官网
根据宝济药业新闻稿,KJ103 是一款全球首创、低免疫原性的重组免疫球蛋白 G(IgG)降解酶,用于治疗由病理性 IgG 抗体介导的多种免疫性疾病。该产品通过特异性切割并降解血液循环中的病理性 IgG 抗体,抑制免疫应答激活,为抗体介导的自身免疫性疾病提供了靶向、快速的治疗新选择。
2026 年 3 月,宝济药业宣布 KJ103 在高度致敏肾移植患者中开展的 III 期临床试验已完成所有受试者的主体随访工作。这是一项多中心、单臂临床研究,于 2025 年 8 月启动,旨在进一步验证 KJ103 在降低患者体内人类白细胞抗原(HLA)抗体水平、促进成功移植方面的临床价值。
研究结果显示,KJ103 在患者中表现出良好的安全性和耐受性,能够快速、有效地降低或清除 HLA-I 类及 HLA-II 类抗体,为高度致敏患者实现成功移植提供了有力支持。
在自身免疫性疾病领域,宝济药业正全面推进多适应症开发战略。除了上述肾移植排斥反应适应症,KJ103 正开展的适应症还包括抗肾小球基底膜病(抗 GBM 病)、吉兰-巴雷综合征(GBS)。其中,抗 GBM 病适应症已于 2025 年 7 月获得 BTD 认定,于同年 10 月完成 II 期临床试验,并于 2026 年 1 月召开了 III 期临床启动会;针对 GBS 的 II 期临床试验也已于 2025 年 11 月启动。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..