1 月 29 日,CDE 官网公示,恒瑞 HRS-4642 注射液拟纳入突破性治疗品种,适应症为联合吉西他滨和紫杉醇(白蛋白结合型)用于携带KRAS G12D突变的晚期或转移性胰腺癌的一线治疗。根据 Insight 数据库, HRS-4642 是全球首个进入 III 期临床的 KRAS G12D 抑制剂。
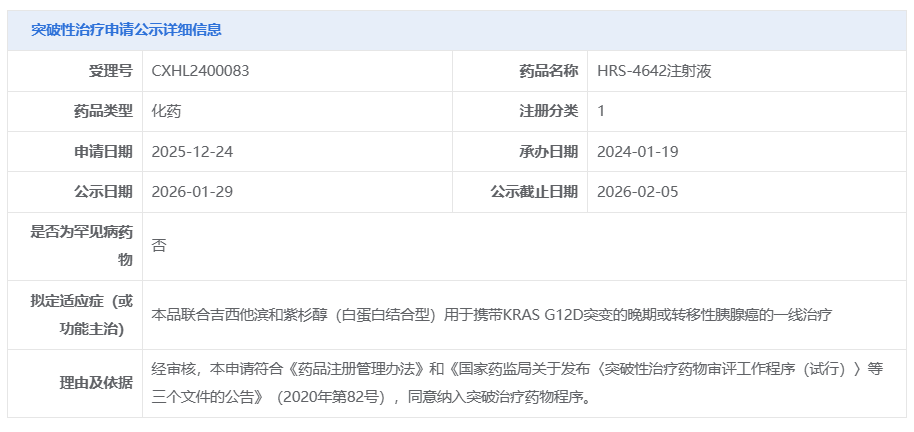
截图来源:CDE 官网
HRS-4642 是一种高选择性、长效、非共价 KRAS G12D 抑制剂,能够特异性结合 KRAS G12D,进而抑制 MEK、ERK 蛋白的磷酸化,发挥抗肿瘤作用。
在 2025 年 ESMO 大会上,恒瑞以口头报告的形式披露了一项该药的 Ib/II 期临床研究结果。截至 2025 年 4 月 10 日,该研究共纳入 31 例胰腺癌患者。30 例初治患者中,确认的 ORR 为 63.3%,DCR 为 93.3%。安全性方面,未发生导致治疗终止的治疗相关的不良事件。
研究结果表明,HRS-4642 联合 AG 方案在晚期 KRAS G12D 突变型胰腺导管腺癌(PDAC)中显示出令人鼓舞的抗肿瘤活性和可控的安全性。长期疗效和安全性数据的随访正在进行中。
2025 年10 月,恒瑞已在国内启动一项随机、对照、双盲、多中心 III 期临床研究,旨在评价 HRS-4642 联合吉西他滨+白蛋白结合型紫杉醇(AG)方案对比安慰剂联合 AG 方案一线治疗携带 KRAS G12D 基因突变的晚期或转移性胰腺癌的有效性和安全性。
Insight 数据库显示,目前全球范围内共有超 40 款 KRAS G12D 抑制剂进入临床阶段。进度最快的在 III 期临床阶段,分别为恒瑞的 HRS-4642 和劲方医药的 GFH375 。其中 ,恒瑞的 HRS-4642 是全球首个进入 III 期临床的 KRAS G12D 抑制剂。
胰腺癌是一种高度恶性的消化系统肿瘤,5 年生存率<10%,多数病人确诊时已处于局部进展期或远处转移阶段,素有「癌中之王」之称。其中,胰腺导管腺癌(PDAC)是最主要的病理类型,占比约 85% 至 90%。
胰腺癌的主要驱动因素是 KRAS 基因突变,约 90% 的患者携带 KRAS 突变,其中大多数突变位于第 12 密码子,最常见突变类型为 G12D(35%~40%)。因此,KRAS G12D 抑制剂有望为这类患者提供一种新的治疗选择。
关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..协会党支部组织党日主题学习会
协会党支部组织党日主题学习会 --..