11 月 28 日,药物临床试验登记与信息公示平台官网显示,神州细胞登记了一项 SCTB14 治疗驱动基因阴性、TPS≥10% 的局部晚期或转移性非小细胞肺癌的 III 期临床试验。
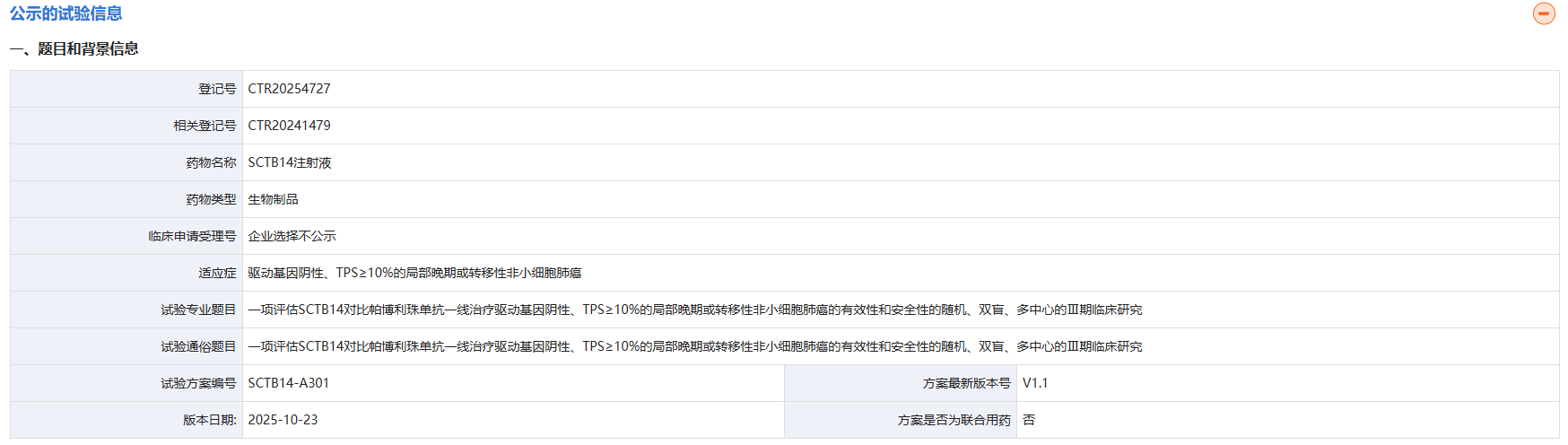
截图来源:临床试验登记与信息公示平台
本次启动的是一项随机、双盲、多中心的 III 期临床研究,旨在评估 SCTB14 对比帕博利珠单抗一线治疗驱动基因阴性、TPS≥10% 的局部晚期或转移性 NSCLC 的有效性和安全性。该试验拟在国内入组 246 人,主要终点是由 BICR 基于 RECIST v1.1 评估的 PFS。关键次要研究目的是 OS。
SCTB14 是一款 PD-1/VEGF 双抗,今年上半年启动了 2 项 II/III 期临床,分别针对非鳞状非小细胞肺癌和非小细胞肺癌。本次是启动的首个 III 期临床。
nsight 数据库显示,除了已经获批上市的依沃西单抗(康方/Summit)以外,神州细胞的 SCTB14 是第三款进入 III 期临床的 PD(L)1/VEGF 双抗,此前还有三生/辉瑞的 SSGJ-707 和普米斯(被 BioNTech收购)/BMS 的普密妥米单抗。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..