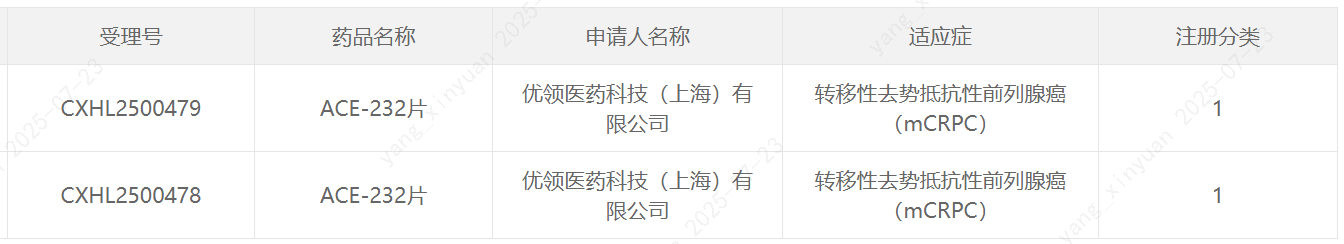
7月22日,中国国家药监局药品审评中心(CDE)官网公示,优领医药(Acerand)申报的1类新药ACE-232片获批临床,拟开发治疗转移性去势抵抗性前列腺癌(mCRPC)。根据优领医药公开资料,这是一款新型CYP11A1抑制剂。
ACE-232是一种新型、高选择性的CYP11A1抑制剂。CYP11A1是类固醇激素合成的关键酶,ACE-232通过抑制该酶来阻断体内雄激素及其他类固醇激素的生成,有望为激素依赖型癌症(如前列腺癌)患者提供一种全新的治疗选择。该产品能克服对雄激素受体(AR)通路抑制剂(ARPI,阿比特龙或恩杂鲁胺)耐药的AR基因变异(AR-LBD突变或AR扩增)。
优领医药在2025年美国癌症研究协会(AACR)年会上公布的临床前数据显示,与目前处于临床后期开发阶段的对比化合物相比,ACE-232在体外抑制CYP11A1活性方面表现出显著更高的效力。多种动物模型中的药代动力学研究表明,ACE-232半衰期长、PK曲线平缓,有望实现在临床每日一次的便捷给药方案下,既达到更加深入持久的临床疗效,又能减少由于血药浓度波动所致的临床副作用。在多种前列腺癌模型中,包括对当前治疗(如阿比特龙和恩杂鲁胺)产生耐药的模型,ACE-232展示了令人鼓舞的抗肿瘤活性。
此外,ACE-232的临床前安全性评价表现出色。全面的安全性评估显示其脱靶效应极小,并且大鼠和犬的GLP毒理学研究展现了相当大的安全治疗窗口。这些数据展示了ACE-232作为下一代激素依赖型癌症疗法的潜力。
美国FDA已于2025年1月批准了ACE-232的IND申请。今年6月,优领医药宣布ACE-232的1期首次人体临床试验完成首例病人入组。这项试验针对转移性去势抵抗性前列腺癌(mCRPC)患者开展。这项多中心1期研究于美国和中国同步开展。研究分为剂量递增阶段(Part IA)和剂量优化阶段(Part IB)两部分,主要目的是评估ACE-232的安全性、耐受性、药代动力学(PK)、药效学(PD)及初步疗效,并确定2期推荐剂量(RP2D)。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..