6月6日,阿斯利康宣布,阿可替尼与维奈克拉(联合或不联合奥妥珠单抗)的固定疗程方案已在欧盟获得批准,用于治疗先前未接受治疗的慢性淋巴细胞白血病(CLL)成年患者。 据悉,该批准基于关键Ⅲ期AMPLIFY研究结果。这是一项随机、全球、多中心、开放标签的Ⅲ期临床试验,旨在评估阿可替尼+维奈克拉±奥妥珠单抗对比研究者选择的化学免疫疗法,用于既往未经治疗且无del(17p)或TP53突变的CLL成年患者的疗效和安全性。研究的主要终点是由独立审查委员会(IRC)评估的阿可替尼+维奈克拉组的PFS。 6月5日,三生国健宣布,其自主创新研发的重组抗IL-1β人源化单克隆抗体注射液SSGJ-613 急性痛风性关节炎适应症已向NMPA递交上市申请并获受理。新闻稿指出,目前我国尚无IL-1β同靶点药物上市。 主要分析结果显示,SSGJ-613在急性痛风性关节炎疼痛缓解和预防复发方面达到双主要疗效终点。其在缓解急性痛风性关节炎受试者的急性疼痛方面与阳性对照药物复方倍他米松注射液的作用相当,此外在预防急性痛风复发方面显著优于阳性对照药物。 同时,SSGJ-613表现出良好的安全性和耐受性,常见不良事件均在预期范围内,与同靶点IL-1β单抗药物相比,未发现新的安全性信号。 据CDE官网近日公示,荣昌生物申报的注射用维迪西妥单抗新适应症上市申请获得受理。根据荣昌生物公开资料,本次申报上市的适应症为治疗HER2低表达乳腺癌。 截图来源:CDE官网 公开资料显示,维迪西妥单抗为一款HER2靶向抗体偶联药物(ADC),通过“精准爆破”机制,不仅能杀伤HER2高表达肿瘤细胞,还可通过“旁观者效应”攻击邻近HER2低表达细胞。 该产品此前已有三个适应症在中国获批上市,分别适用于至少接受过2种系统化疗的 HER2过表达局部晚期或转移性胃癌患者、既往接受过含铂化疗且HER2过表达局部晚期或转移性尿路上皮癌患者、既往曾接受过曲妥珠单抗或其生物类似药和紫杉类药物治疗的HER2阳性存在肝转移的晚期乳腺癌患者。AZ联合疗法首次获批上市
国内第二款,三生国健痛风新药国内报上市
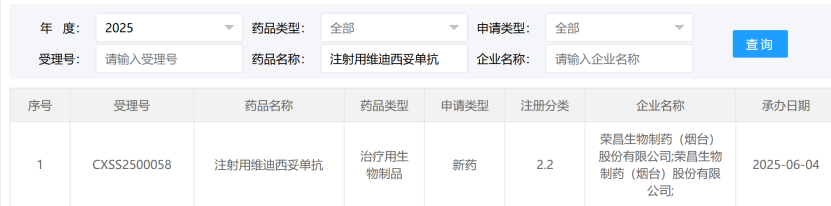
荣昌生物ADC新适应症申报上市
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..