3月25日,中国国家药监局药品审评中心(CDE)官网公示,恒瑞医药申报的氟唑帕利胶囊和甲磺酸阿帕替尼片拟纳入突破性治疗品种,针对适应症为:氟唑帕利单药或联合阿帕替尼治疗gBRCA突变的HER2阴性乳腺癌。
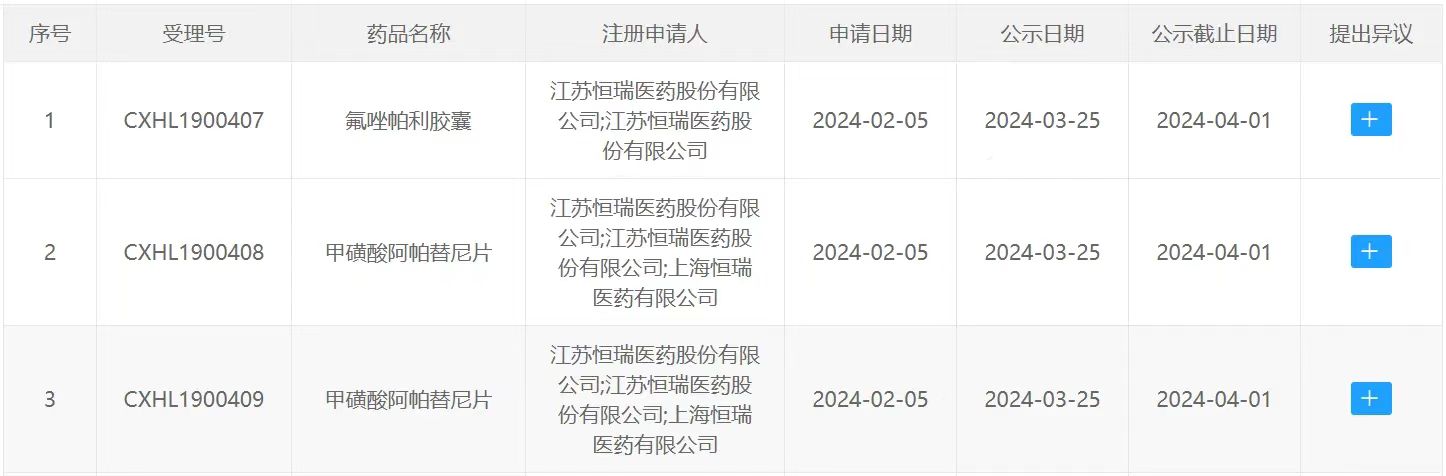

截图来源:CDE官网
氟唑帕利是恒瑞医药研发的1类创新药,为一种新型口服PARP抑制剂。该药已经在中国获批用于胚系BRCA1/2(gBRCA1/2)突变的铂敏感复发性卵巢癌治疗,以及铂类敏感复发性卵巢癌维持治疗,无论胚系BRCA1/2突变状态如何。
阿帕替尼是恒瑞医药研发一种高选择性的靶向血管内皮细胞生长因子受体2(VEGFR2)的抗血管生成药物,已经在中国获批单药治疗晚期胃腺癌或胃-食管结合部腺癌、晚期肝细胞癌,以及联合卡瑞利珠单抗治疗不可切除或转移性肝细胞癌。此外,它在卵巢癌和乳腺癌等多种实体肿瘤中均显示良好的活性和安全性。
根据恒瑞医药公开资料介绍,抗血管生成药物可以引起肿瘤微环境缺氧,导致遗传不稳定性和BRCA1/2的下调,从而增强对PARP抑制剂的敏感性。既往研究已经证明,抗血管生成药物联合PARP抑制剂,可改善患者的无进展生存期(PFS)。
根据中国药物临床试验登记与信息公示平台官网,氟唑帕利单药或联合阿帕替尼的多个适应症开发已处在3期临床研究阶段。其中,一项氟唑帕利或氟唑帕利联合阿帕替尼治疗乳腺癌的3期研究正在进行中。该研究第一阶段主要目的为评价联合疗法在转移性乳腺癌中的耐受性,以及相比于研究者选择的化疗的优效性。
值得一提的是,2023年11月,恒瑞医药宣布氟唑帕利联合阿帕替尼治疗晚期卵巢癌和三阴性乳腺癌的1期研究结果发表于BMC Medicine。该研究由北京大学肿瘤医院李惠平教授和高雨农教授团队共同开展。研究结果显示,在最高剂量水平,即氟唑帕利100mg联合阿帕替尼500mg治疗组中,客观缓解率(ORR)为50%;gBRCA突变的患者ORR和中位无进展生存期(PFS)均优于gBRCA野生型患者。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Mar 25, 2024, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]恒瑞创新药氟唑帕利联合阿帕替尼治疗卵巢癌和乳腺癌研究发表于BMC Medicine. Retrieved Oct
11, 2023, from https://mp.weixin.qq.com/s/4cy8E8uCHKFmHG-n4xG7dw
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..