2024年3月19日,阿斯利康(“AstraZeneca”)宣布,已达成收购 Fusion Pharmaceuticals(简称“Fusion”)的最终协议。此次收购补充了阿斯利康领先的肿瘤学产品组合,包括II期项目FPI-2265,一种针对转移性去势抵抗性前列腺癌 (mCRPC) 患者的潜在新疗法。
根据协议条款,阿斯利康将通过一家子公司,以每股 21.00 美元的现金价格收购 Fusion 的所有已发行股票,外加在实现特定监管里程碑时支付的每股3.00美元的不可转让或有价值现金权。整个交易对价约为24亿美元。
一
关于Fusion
Fusion是一家临床阶段的肿瘤学公司,专注于开发作为精准药物的下一代放射性药物。Fusion是靶向α粒子疗法的行业领导者,利用的是一种能放射α粒子的医学同位素,将靶向癌细胞的抗体与α粒子“绑定”在一起,精准狙击癌细胞。
利用其独创了Fast-Clear连接子技术,Fusion将发射α粒子的同位素连接到各种靶向分子,以便选择性地将发射α粒子的有效载荷传递给肿瘤;与传统技术相比,可扩大治疗窗口。目前,此技术应用于不同类别的药物,如抗体、小分子等。
近年来,放射性偶联物(RDC)已成为癌症治疗的一种很有前途的方式。这些药物通过使用抗体、肽或小分子等分子进行精确靶向,将放射性同位素直接传递给癌症细胞。与传统的放射治疗相比,这种方法具有许多潜在的优势,包括最大限度地减少对健康细胞的损伤,并使其能够接触到无法通过外束辐射到达的肿瘤。
目前,公司主要在研药物包括:
Part.1
FPI-2265
FPI-2265是一种靶向前列腺特异性膜抗原(PSMA)的潜在新治疗方法,目前正针对mCRPC患者进行II期试验。
II期研究旨在评估FPI-2265在约60名经过177Lu PSMA放射配体治疗(如PLUVICTO™)后,在具有进展性疾病的mCRPC患者中的三个剂量方案的安全性和有效性。主要终点是安全性和PSA水平下降≥50%的患者比例,次要终点包括客观缓解率(ORR)和影像学无进展生存期(rPFS)。Ⅱ期临床试验预计将于2024年第二季度开始,到年底完成招募。
根据文献和迄今为止报告的TATCIST数据,已知每8周以100 kBq/kg剂量给药是一个安全而有效的剂量方案;目前,FPI-2265已经治疗超过300例患者,包括大约100例经过177Lu-PSMA治疗后进展的患者,仍然可以看到治疗响应。
Part.2
FPI-1434
FPI-1434是一种新型α靶向治疗药物(TAT),由抗IGF-1R人源化单克隆抗体,专有的双功能螯合物和α发射放射性核素锕-225组成。
根据2023 SNMMI 的摘要显示,在剂量递增过程中,FPI-1434血浆暴露量(曲线下面积)随剂量增加而增加;与铟-111成像类似物FPI-1547联用,导致全身暴露量大幅增加。
Part.3
FPI-2068
FPI-2068是一种基于双特异性IgG的临床阶段靶向α疗法(TAT),旨在将Ac-225递送到多种表达EGFR-cMET的实体瘤。EGFR和cMET是经过验证的癌症靶点,在多种肿瘤类型中共表达,包括头颈部鳞状细胞癌、非小细胞肺癌、结直肠癌和胰腺导管腺癌。
临床前研究中,FPI-2068在结直肠和肺肿瘤异种移植小鼠模型中表现出抗肿瘤疗效,单剂量给药FPI-2068可延长肿瘤消退时间;此外,FPI-2068引起DNA损伤反应(DDR)通路的激活和细胞凋亡,表明细胞机制无法修复由α辐射引起的DNA损伤,这与提出的主要作用机制一致。
二
放射性偶联药物
RDC是一种将精准靶向分子 (单抗或多肽/小分子,Ligand) 和强力杀伤因子 (核素,Radioisotope) 用连接臂 (Linker) 螯合剂(Chelator)偶联在一起而设计开发的药物形态;得益于其特殊的作用机制,RDC可实现高精度诊断及在治疗疾病的过程中具有不易耐药等优点,被认为是目前核药靶向治疗领域最具潜力的发展方向之一。
RDC的结构类似于ADC 药物,据简一生物官方公众号,RDC 机制为利用抗体或小分子介导特异性靶向作用,将细胞毒性分子或成像分子如放射性核素递送至靶位置,从而将放射性同位素产生的放射线集中作用于组织局部,在高效精准治疗的同时降低全身暴露对其他组织造成的损伤。核素带来的放射性射线所产生的能量可破坏细胞的染色体,使细胞停止生长,从而消灭快速分裂和生长的癌细胞。
根据靶向配体的不同,可细分为抗体偶联核素药物(ARC)、小分子偶联核素药物和多肽偶联核素药物(PRC),其中多肽偶联核素药物是目前的热门研发方向。
RDC 具备诊疗一体的优势,实现疾病诊断和治疗双赢。在诊断层面,通过连接诊断核素进入人体,利用分子影像方式监测诊断试剂及其靶点结合的位置,这也就意味着看见其靶向需要治疗的肿瘤位置;在治疗层面,同一药物结构加载治疗核素后,相应治疗核药仍然会结合到上述诊断试剂结合的肿瘤靶点上,从而产生治疗效果。具体优势包括:
机制方面:核药依靠直接的核素内照射,可降低肿瘤细胞的放射抵抗的耐药机会。
靶向配体:除了大分子的单抗以外,还可以是体积更小的小分子或多肽等,更容易让RDC 通过渗透作用深入肿瘤内部,更不容易产生耐药。
RDC具有诊疗一体化、潜在适应症广泛、行业壁垒极高等特点,因此成为当前热点,投融资金额不断提升,2022 年全球融资额近7 亿美元。
据肽研社公众号,2016 年以来,FDA一共批准了9 款RDC 药物,涉及6 个新分子实体;其中,Novartis 是该领域的领跑者,拥有多款RDC药物。POINT Biopharma、Telix、ITM、拜耳等也在积极布局RDC赛道,多款肿瘤治疗产品处于临床阶段。
2016年以来FDA审批通过的9款RDC药物
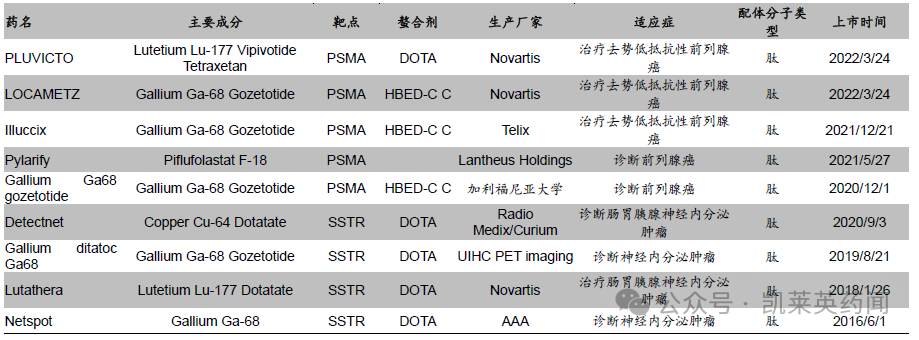
从靶点上看,RDC 药物以靶向前列腺特异性膜抗原(PSMA)的项目居多,同时也涉及在ADC 药物中较受欢迎的Her2 靶标;
在适应症上,RDC 药物主要集中在肿瘤领域。
2022 年,Lutathera、Pluvicto营收分别为4.71、2.71亿美元。Lutathera 上市当年销售额即突破1.6 亿美元,但由于Lutathera 获批的适应症为胃肠胰腺神经内分泌肿瘤,属于罕见肿瘤,市场需求有限,上市后第二年达峰后,基本稳定在约4 亿美元的销售额。Pluvicto在2022年被FDA 获批用于治疗前列腺特异性膜抗原(PSMA)阳性、转移性去势抵抗性前列腺癌(mCRPC)患者,有望接力Lutathera 打开更大市场空间。
参考资料
1、公司官网
2、动脉新医药、汇佳生物、医药宇宙、小核说核药、医药笔记、药智网、简一生物、bioSeedin柏思荟
3、德邦证券、申万宏源、华泰证券、平安证券、国元国际、中信证券
关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..协会党支部组织党日主题学习会
协会党支部组织党日主题学习会 --..