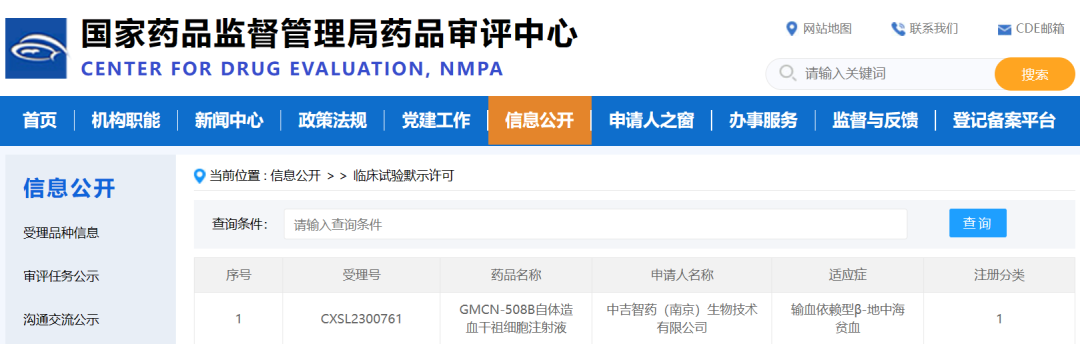
2024年1月26日,中吉智药申报的基因治疗β-地中海贫血药物GMCN-508B的临床试验(IND)申请,获国家药品监督管理局药品审评中心(CDE)默示许可,标志公司正式进入注册临床试验阶段。
此次IND获批,是中吉智药作为专注慢病毒载体和造血干细胞治疗领域的新兴公司,跨越了重要里程碑,标志着中吉智药已经由“科学家”,成功转身为“制药人”。
GMCN-508B的临床试验获批,表明公司创立之初采取 “独立自主,合作共赢”策略是必要的和有效的。同时可预见,公司接下来的基于慢病毒载体和造血干细胞制剂的管线,如a-地贫、丙酮酸激缺乏症“和范可尼贫血症的研究开发,必将游刃有余,更加顺利。
中吉智药的发展,从一开始就离不开合作伙伴的大力支持,在此特别感谢金斯瑞蓬勃、集萃药康、益诺思以及其他服务和物料的供应商伙伴。中吉智药也一直致力于促进行业发展,积极组织和参与各种行业交流,分享各项进展和药物评价工具,广泛开展形式多样的合作,愿尽力与全行业一起发展进步,造福患者。
关于中吉智药
中吉智药(南京)生物技术有限公司(以下简称“公司”)位于南京江北新区生物医药谷,最早于2018年在北京设立研发中心。公司专注于造血干细胞相关疾病,是一家基因治疗创新药物企业。公司已完成多轮融资,步入临床阶段。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..