(四十六)血管造影X射线机:该产品由高压发生器、X射线管组件、限束器、滤线栅、平板探测器、机架、导管床、显示器、显示器吊架、视觉组件、触控平板、控制模块、控制盒、脚踏开关、手闸、图像采集工作站、视频管理工作站、图像高级处理工作站、3D图像处理工作站和附件组成。适用于对血管造影检查、介入手术时提供X射线透视、摄影、血管减影图像和体层图像。
该产品采用9轴机器人DSA,能实现全腹部、全胸部的锥形束成像,解决了传统锥形束CT重建视野小的问题。此外,产品采用计算机视觉技术,实现了一键自动锥形束CT扫描和一键到位,可简化定位和锥形束CT的工作流,减少辐射暴露和术中操作步骤。与传统的医用血管造影X射线机相比,该产品可显著扩大锥形束CT重建视野,减少锥形束CT扫描的操作步骤、操作时间和辐射剂量,预期缩短成像前的准备时间,提高手术效率。
五、其他注册管理情况
(一)境内第二类医疗器械注册审批情况
2022年,各省级药品监管部门共批准境内第二类医疗器械注册32889项,与2021年相比增加4.4%。其中,首次注册13334项,与2021年相比增加2.2%。首次注册项目占全部境内第二类医疗器械注册数量的40.5%。
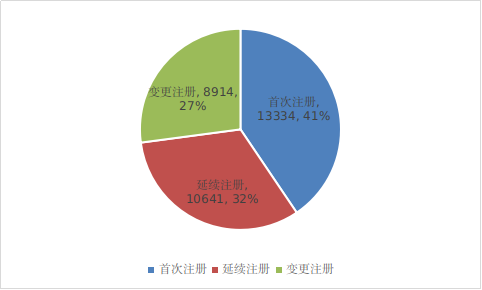
图17 境内第二类医疗器械注册形式比例图
延续注册10641项,与2021年相比减少6.9%,占全部境内第二类医疗器械注册数量的32.4%;变更注册8914项,与2021年相比增加26.6%,占全部境内第二类医疗器械注册数量的27.1%。
境内第二类医疗器械分项注册情况见图17。
从注册情况看,广东、江苏、北京、湖南、浙江、河南、山东、上海、湖北、安徽10省(直辖市)注册的境内第二类医疗器械数量较多。
第二类医疗器械注册具体数据见表1及图18。
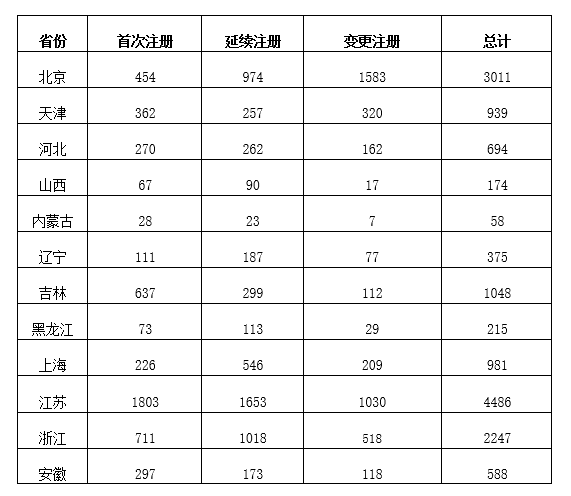
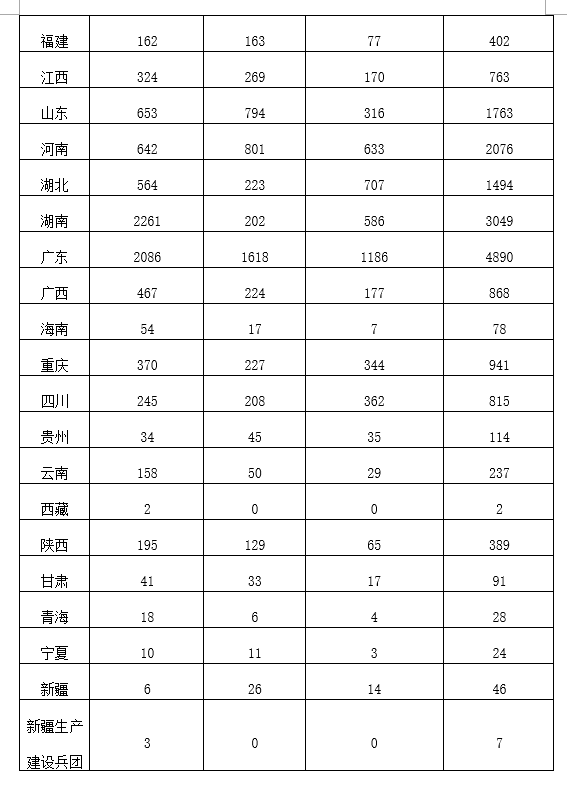
表1 境内第二类医疗器械注册表
从首次注册情况看,湖南、广东、江苏、浙江、山东、河南、吉林、浙江、湖北、广西10省(直辖市)首次注册的境内第二类医疗器械数量较多。各省第二类医疗器械首次注册数量排序图见图19。
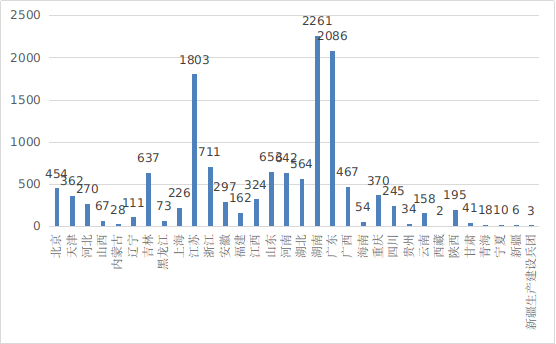
图18 各省第二类医疗器械注册数据图
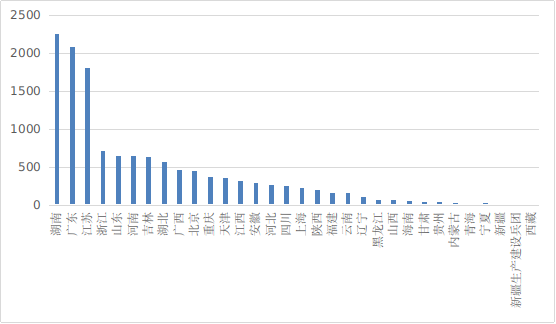
图19 各省第二类医疗器械首次注册排位图
(二)第一类医疗器械备案情况
2022年,国家药监局依职责共办理进口第一类医疗器械备案数量2023项,与2021年相比增加9.1%。
全国设区的市级药品监管部门依职责共办理境内第一类医疗器械备案数量28508项,与2021年相比增加6.5%。此外,2022年各省取消一类备案13917项。
(三)登记事项变更/变更备案情况
2022年,国家药监局依职责共办理进口第二、三类和境内第三类医疗器械变更备案5390项,与2021年相比增加17.1%。
其中,境内第三类医疗器械变更备案3435项,进口第二类、三类医疗器械变更备案1995项。
各省级药品监管部门依职责共办理境内第二类医疗器械变更备案11638项,与2021年相比增加8.5%。
(四)医疗器械临床试验机构备案情况
自2018年1月1日《医疗器械临床试验机构条件和备案管理办法》颁布实施以来,全国共计1177个机构完成了医疗器械临床试验机构备案工作,比2021年增加9.6%。
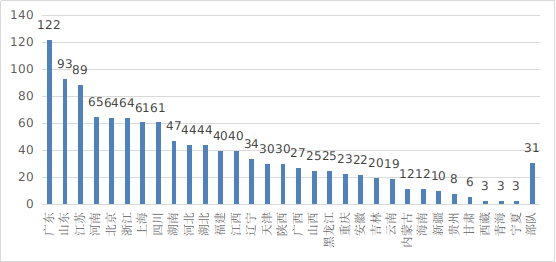
图20 全国医疗器械临床试验机构备案数量
其中广东、山东、江苏、河南、北京和浙江临床试验机构备案数量居全国前五名。全国医疗器械临床试验机构分布情况见图20。
注:本报告的数据统计自2022年1月1日至2022年12月31日。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..