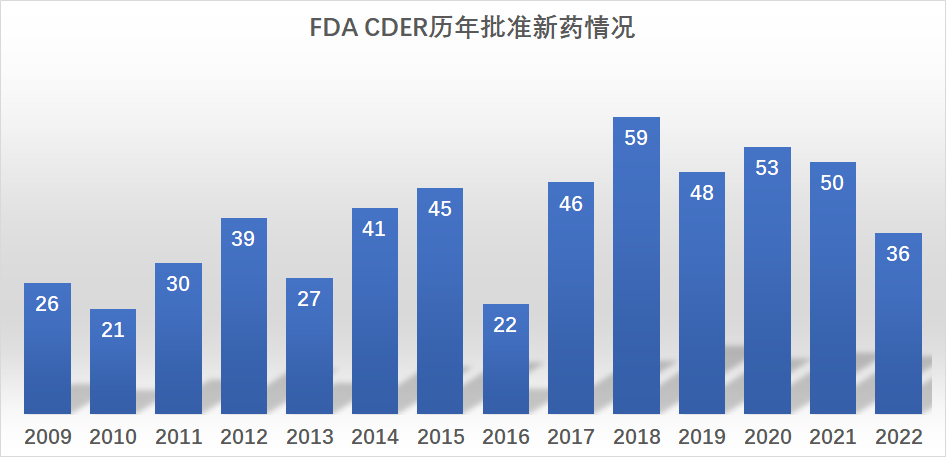
2022年,FDA药物评估和研究中心(CDER)共批准36种新分子实体和新生物产品,该数字创造了2017年以来6年新低。其中作为近年来备受关注的单克隆抗体类别,FDA共批准了10种产品,占总数的28%。肿瘤适应症仍旧是批准最大治疗领域,获批11种药物。
就FDA批准新药的市场潜力而言,礼来的葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂Mounjaro无疑最被看好,销售额峰值可能达到惊人的250亿美元。
细胞和基因疗法继续发力。FDA生物制品评价和研究中心(CBER)在2022年批准了3种基因疗法(Zynteglo、Skysona、Hemgenix)和一种Car-T细胞疗法Carvykti。美国FDA预计,到2025年FDA每年将会批准10~20款基因与细胞治疗产品,这一预测有望实现。FDA还批准首个粪便微生物疗法Rebyota。

四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..