昨晚9点,康方生物发布一则重磅公告:康方生物将授予Summit Therapeutics于美国、加拿大、欧洲和日本的开发和商业化依沃西(PD-1/VEGF双特异性抗体)的独家许可权;康方生物保留依沃西除以上地区之外的开发和商业化权利,包括中国。
基于此协议及条款,康方生物将获得5亿美元的首付款以及最高50亿美元的总交易金额,包括开发,注册和商业化里程碑款项付款。50亿美元的授权交易总额创下了中国创新药license out之最,比此前百济神州授权诺华Ociperlimab(TIGIT抑制剂)还高出21亿美元。
“在公司发展的特定阶段、特定时间,只要合作对于双方是有利的,就要毫不犹豫地拥抱合作。”康方生物创始人、董事长兼CEO夏瑜博士在接受新康界采访时表示,康方生物坚持自主研发,同时保持高效、多元、开放的开发策略,联合优势资源加速产品的创新推进是康方生物的策略之一。
图表1:近年国内药企重磅交易授权事件(总额>10亿美元)
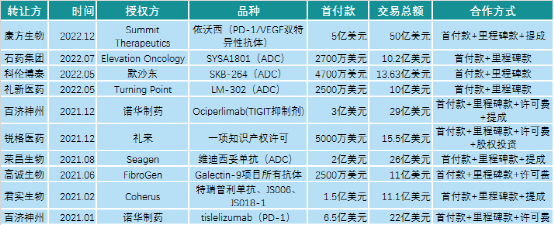
数据来源:中康FIC Intelligence数据库
从上图可以看出,自2021上半年以来,重磅的授权交易主要集中在ADC药物,特别是荣昌生物维迪西妥单抗以最高26亿美元的授权交易金额一举创下当时的授权记录。而此次康方生物50亿美元依沃西的授权,势必会引爆双抗市场。
依沃西是康方基于TETRABODY平台同类首创的PD-1/VEGF双抗,也是全球首个进入III期临床的PD-1/VEGF双抗。此前在肾癌、非小细胞肺癌、肝癌等多种肿瘤中, PD-1/PD-L1与VEGF单靶点药物的联用疗效突出。
康方生物已开展两项关于依沃西的III期临床研究,包括:一项在一线非小细胞肺癌中对照帕博利珠单抗的头对头临床研究;另一项在克服非小细胞肺癌患者EGFR-TKI 耐药的临床研究。如下图所示:
图表2:康方生物依沃西临床进展情况
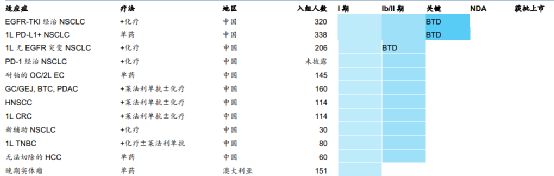
数据来源:公开资料、中康产业研究中心整理
另外,依沃西是国内肺癌领域唯一获得3个突破性治疗药物认定,也是国内唯一在PD-1/L1耐药的肺癌治疗领域获得突破性治疗药物认定的创新药。基于依沃西在肺癌领域的全面覆盖与更高的疗效与安全性潜能,市场上预计销售峰值将达60亿元。
值得注意的是,此次的购买方Summit Therapeutics是一家市值只有1.58亿美元,账上现金只有1.2亿美元的公司。但这一点不值一虑,Summit的CEO和最大股东Duggan在医药领域极具影响力,曾靠4300万美元投资BTK抑制剂依鲁替尼而获得数十亿美元的回报,足以证明Duggan的资金实力和投资眼光。
事实上,康方生物在发展的不同阶段,先后与美国默克、东瑞制药、GE,以及中国生物制药开展了不同形式的合作,都是公司在特定时点的最佳选择。此次与Summit授权合作能否成为又一经典,值得期待。
康方生物在授权的同时,也着手准备在A股科创板上市,在补齐资金这一块短板后,双抗龙头康方生物正向bigpharma大步迈进。
四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..四川省医药保化品质量管理协会召开第七
2025年12月17日,四川省医药保化品..协会党支部组织党日主题学习会
协会党支部组织党日主题学习会 --..关于相关收费标准的公示
根据四川省医药保化品质量管理协会..协会党支部组织党日主题学习会
协会党支部组织党日主题学习会 --..