通过开发同时激动多个与代谢相关的靶点来治疗代谢性疾病是目前新药研发最新趋势,当前全球各大药企已将降糖药研发的重点聚焦于此。
在国内,信达 GLP-1R/GCGR 双靶点激动剂 Mazdutide(IBI362)曾以亮眼的数据引起众多业内人士关注,而信达也在积极加快其开发进度。
10 月以来,信达同步启动了 3 项 Mazdutide 用于 2 型糖尿病以及肥胖适应症的 III 期临床,足以看出信达对该产品的信心。
2 型糖尿病:
两项 III 期临床研究同步启动
11 月 7 日,据 ClinicalTrials.gov 显示,信达 GLP-1R/GCGR 双靶点激动剂 Mazdutide(IBI362) 登记了一项 III 期临床试验(登记号:NCT05606913)。
这是一项针对 2 型糖尿病患者头对头度拉糖肽的随机、平行、双盲 III 期临床研究,研究计划共入组 720 例受试者,目前暂未开始招募,预计于 11 月 23 日开始试验,并于 2025 年 2 月完成。
此前,信达已在 CDE 临床试验平台登记了一项 Mazdutide 用于糖尿病患者的 III 期临床试验,并于 11 月 4 日首次公示信息(登记号:CTR20222875)。不过,有所区别的是,该项研究的对照组仅为安慰剂,研究主要目的为评估不同剂量 Mazdutide 在受试者中的有效性和安全性。
针对 2 型糖尿病,信达在今年 7 月披露在中国患者 II 期临床研究数据显示:Mazdutide 有显著的降糖、减重双重疗效和多重代谢获益。
这是一项多中心、随机、安慰剂/度拉糖肽对照的 II 期临床试验(登记号:NCT04965506 )。结果显示,与安慰剂相比,连续给药 20 周后,Mazdutide 各剂量组均能显著降低受试者 HbA1c 水平。在受试者的体重管理方面,与安慰剂相比,Mazdutide 各剂量也均可显著降低体重,且呈现剂量依赖性。
其中,Mazdutide 6.0 mg 组 HbA1c<7.0% 且体重较基线下降 ≥5%的受试者比例高达52.2%(度拉糖肽 1.5 mg 组为 14.0%,安慰剂组为 0%)。
此外,Mazdutide 还可降低空腹血糖、餐后血糖、血压、低密度脂蛋白胆固醇和甘油三酯等指标,并改善胰岛素敏感性,为患者带来全面获益。
肥胖领域:
启动一项 III 期临床研究
除糖尿病外,信达也在同步开展 Mazdutide 针对减重的研究,而两者的开发进度几乎一致,今年 10 月,信达首次启动了一项 III 期临床 GLORY-1 研究,以评估与安慰剂相比,Mazdutide 对中国超重或肥胖患者体重的影响(登记号:CTR20222567),试验分组及主要终点指标如下:
根据此前披露的研究数据显示,Mazdutide 在减重领域同样具有非常大的潜力。
信达 6 月披露了一项入组 248 受试者的 II 期临床研究(登记号:NCT04904913 )数据,结果显示,Mazdutide 各剂量在中国超重或肥胖受试者中展现出显著的减重疗效,呈现剂量依赖性。其中,6.0mg 组数据显示,Mazdutide 持续给药 24 周后,体重下降 11.57%;且与安慰剂相比,可带来 12.6% 的体重降幅。
同时,在此次 II 期研究中已经同步实现了自动注射器的应用,极大改善了研究受试者生活质量与依从性。
而根据今年 10 月在柳叶刀子刊发表的 Mazdutide 在中国超重或肥胖受试者中的多次给药剂量递增的 1b 期临床研究高剂量队列的研究结果数据显示:9mg 剂量组 Mazdutide 给药 12 周后,受试者体重变化率为 -11.7%。
根据信达对 Mazdutide 的开发计划,除 2 型糖尿病以及肥胖症外,后续还将拓展用于非酒精性脂肪性肝炎的适应症。
11 款 GLP-1R 多靶点激动剂
国内进入临床阶段
在国内,据 Insight 数据库显示,除 Mazdutide 外当前共有 10 款 GLP-1R 多靶点激动剂进入临床阶段。
进展最快的是礼来 GIP/GLP-1R 双重激动剂每周给药一次的替尔泊肽注射液(Tirzepatide),目前处于上市申请阶段。Tirzepatide 已于今年 5 月获 FDA 批准上市,成为首款治疗 2 型糖尿病的 GLP-1R 双靶点降糖药。该产品曾在大型 III 期临床中头对头击败司美格鲁肽,表现十分亮眼。
此外,阿斯利康 GLP1R/GCGR 双重激动剂 Cotadutide 也已处于 III 期临床阶段。而国产企业中翰森制药、东阳光药业等布局的 GLP-1R 多靶点激动剂均已进入临床阶段。
值得一提的是,礼来还在布局三靶点降糖药,其在研的 GIPR/GLP-1R/GCGR 三重激动剂也已于今年 9 月在国内启动临床(登记号:CTR20222436)。>>>替尔泊肽之后,礼来三靶点降糖药来了!国内临床试验已启动
国内进入临床阶段的 GLP-1R 多靶点激动剂(不包括复方制剂)
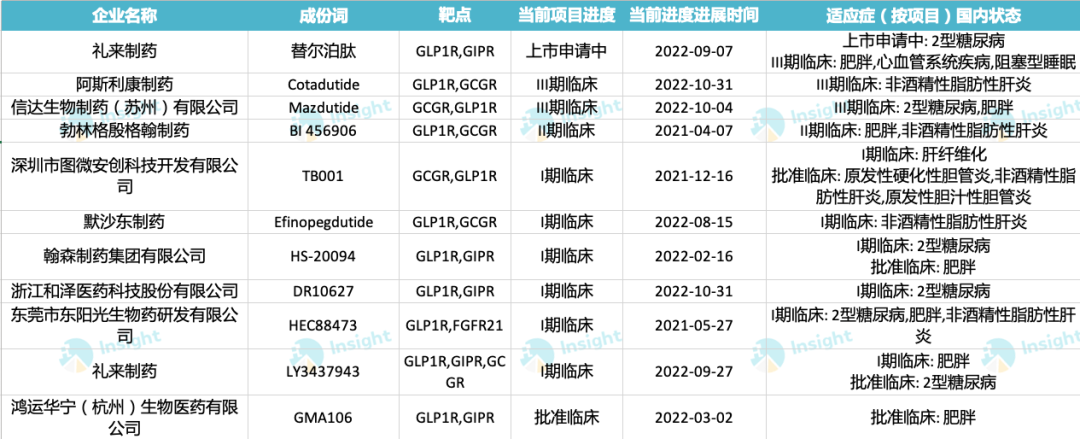
来自:Insight 整理(PS:手动整理如有纰漏请指正)
四川省医药保化品质量管理协会召开第七
2026年6月8日,四川省医药保化品质..关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..