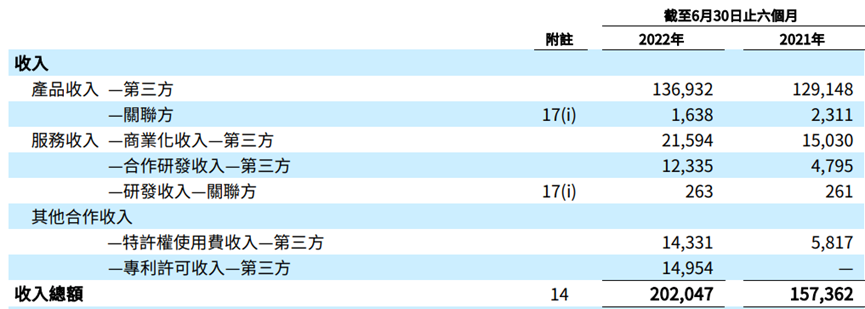
8月1日,和黄医药公布2022年H1财报业绩,总营收2.02亿美元(2021年H1:1.574亿美元),同比增长28%;肿瘤/免疫业务综合收入为9110万美元(2021年H1:4290万美元),同比增长113%;净亏损1.629亿美元(2021年H1:1.024亿美元)。
研发投入1.817亿美元(2021年H1:1.231亿美元),同比增长48%,其中在中国的研发开支为9810万美元(2020年H1:6380万美元),在美国和欧洲的国际临床和法规事务团队产生了8360万美元(2021年H1:5930万美元)的开支;销售及行政开支为7980万美元(2021年H1:5480万美元),同比增长46%。
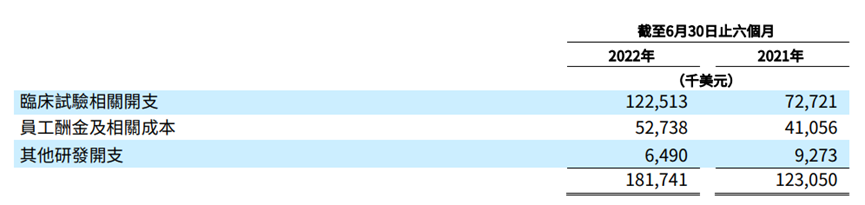
肿瘤免疫业务的快速增长,主要得益于爱优特(呋喹替尼、HMPL-013)、苏泰达(索凡替尼、HMPL-012)及沃瑞沙(赛沃替尼、HMPL-504)销售额增加以及达唯珂(他泽司他)的获批上市。
呋喹替尼(爱优特)是一种高选择性的口服VEGFR1/2/3激酶抑制剂,旨在提高激酶选择性以减少脱靶毒性,从而提高耐受性;2018年在国内上市。其2022年上半年生产收入、推广及营销服务收入及特许权使用费收入3600万美元(2021年H1:2980万美元),同比增长21%,乃因和黄医药自有销售团队带动的市场销售额为5040万美元(2021年H1:4010万美元),同比增长26%。
索凡替尼(苏泰达)是一种口服酪氨酸激酶抑制剂,可抑制VEGFR和FGFR从而阻断肿瘤血管生成,还可抑制CSF-1R从而调节肿瘤相关巨噬细胞以促进人体对肿瘤细胞的免疫应答;2021年1月在国内上市,被批准用于治疗晚期胰腺外(非胰腺)神经内分泌瘤患者,2021年6月被批准用于治疗胰腺神经内分泌瘤患者。其2022年上半年销售额为1360万美元(2021年H1:800万美元),同比增长69%。此外,索凡替尼于2022年1月起纳入国家医保目录。
2020年5月,和黄医药向FDA递交了索凡替尼用于治疗胰腺和非胰腺神经内分泌瘤的上市申请。但是,该申请被FDA驳回了。
赛沃替尼(沃瑞沙)是一种高选择性的口服MET抑制剂,2021年6月在国内附条件批准上市,7月正式上市。得益于阿斯利康于2021年底推出的患者用药援助计划,赛沃替尼2022年上半年销售额增长至2330万美元(2021年H1:零)。
他泽司他(达唯珂)是一种EZH2甲基转移酶抑制剂,2022年6月在海南获批上市,用于治疗某些上皮样肉瘤和滤泡性淋巴瘤患者,其销售额为10万美元。
目前,和黄医药拥有约1800人的肿瘤/免疫业务团队,其中创新药研发人员约960名,肿瘤业务商业化团队820人,覆盖约3000家肿瘤医院。
在产品管线方面,和黄医药已有3款创新药获批上市,分别是索凡替尼、呋喹替尼和赛沃替尼,1款获批于海南先行区上市,3款处于全球后期开发阶段,共13款进入临床阶段。
此外,和黄医药肿瘤管线处于早期开发阶段候选药物还有安迪利塞(HMPL-689,PI3Kδ抑制剂)、索乐匹尼布(HMPL-523,Syk抑制剂)、他泽司他(EZH2甲基转移酶抑制剂)、HMPL-453(FGFR 1/2/3抑制剂)、HMPL-760(BTK抑制剂)、HMPL-306(IDH 1/2抑制剂)、HMPL-295(ERK抑制剂)、HMPL-760 (BTK抑制剂)、HPML-653(CSF-1R抑制剂)、HMPL-A83(抗CD47单抗)。
此外,2021年1月,和黄医药与创响生物达成战略合作伙伴关系,共同开发4款临床前候选化合物,其中2款的临床试验申请已于2022年提交。
2022年,和黄医药预计已上市的3款药物销售额为1.6-1.9亿美元,增加投资支持全球临床试验和组织扩张。同时,为支持现金需求,和黄医药继续积极进行有关出售潜在非核心资产(如上海和黄药业)的讨论,及继续评估在其他资本市场,如在上海证券交易所的科创板的上市机会。
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..