乳腺癌如今已成为威胁女性健康的头号杀手,2020年中国新发癌症中,乳腺癌患者超过41万。新确认的女性癌症患者中,每5人中就有1人是乳腺癌。在这个需求巨大且极大未被满足的现状下,CDK4/6抑制剂承载了患者太多的期望。
进口CDK4/6抑制剂高昂的价格让很多人头疼,不过这种情况正在被迅速改善,朝着乐观的方向积极发展。特别是在我国科学家的努力下,便宜的CDK4/6抑制剂脚步已经越来越近。
令人欣慰的进展
今年以来,特别是近期,CDK4/6抑制剂的研发获得了诸多进展。
11月4日,国际四大医学期刊之一的《自然医学》(Nature Medicine)在线发表了恒瑞医药的CDK4/6抑制剂达尔西利(SHR6390)联合氟维司群治疗既往内分泌治疗后疾病进展的HR+/HER2-晚期乳腺癌的多中心、随机、双盲III期临床研究中期分析结果报告。
研究结果显示,达尔西利+氟维司群组与安慰剂+氟维司群组相比,无进展生存期(PFS)显著延长。该研究结果表明,对于内分泌治疗后进展的激素受体阳性、HER2阴性晚期乳腺癌患者,达尔西利联合氟维司群可以作为新的治疗选择。
在今年4月,恒瑞医药已经将达尔西利递交新药上市申请,并被纳入突破性治疗品种和优先审评。恒瑞关于SHR6390相关项目累计投入研发费用超过2.7亿元。
10月22日,诺华的CDK4/6抑制剂琥珀酸利柏西利片上市申请获国家药监局受理。
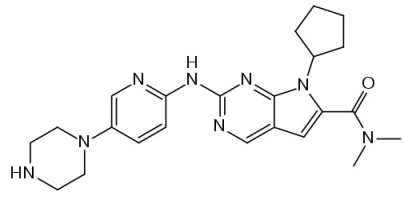
利柏西利结构式
来源:https://3g.163.com/w_x/article/GMUL33HH0534Q32Z.html
琥珀酸利柏西利片(Ribociclib)是全球第2款获批上市的CDK4/6抑制剂。2017年3月该药获FDA批准上市,商品名为Kisqali,同年8月在欧盟获批,2020年其全球销售额达到6.87亿美元。
截至目前,利柏西利获FDA批准的适应症包括:与芳香化酶抑制剂联合,用于绝经前/围绝经期以及绝经后激素受体(HR)阳性、HER2阴性晚期或转移性女性乳腺癌患者;与氟维司群联用作为初始内分泌治疗或用于初始内分泌治疗失败疾病进展的HR+,HER2-晚期或转移性女性乳腺癌患者。
来源:诺华官网
在今年6月举办的ASCO年会上,诺华公布了利柏西利乳腺癌III期MONALEESA-3试验的最新总生存期结果。
结果显示:在中位随访56.3个月后,氟维司群单药组的中位总生存期为41.5个月,而Kisqali+氟维司群组的中位总生存期达到了53.7个月,这是HR+/HER2-转移性乳腺癌绝经后女性治疗方面报告的最长总生存期数据。
而在9月份举办的ESMO 2021上,发布CDK4/6抑制剂动向的有一家来自国内的药企----甘李药业,其该产品的研发代号为GLR2007,临床前体外研究结果表明,GLR2007对CDK4和CDK6的抑制作用分别是辉瑞哌柏西利的33.1和3.8倍。
据悉,甘李药业的这款CDK4/6抑制剂已分别在2021年1月和4月获得FDA\EMA的孤儿药资格认定,用于治疗胶质瘤。10月19日,GLR2007首次在国内启动一项Ib/II期临床,用于晚期实体瘤。
而在今年更早之前,3月,嘉和生物宣布,其CDK4/6抑制剂GB491(Lerociclib)的两项临床试验申请已获得国家药监局批准,一项为一线联合来曲唑治疗既往未经过系统性抗肿瘤治疗的HR阳性、HER2阴性晚期乳腺癌患者的多中心、开放标签、1b期临床试验;另一项为二线联合氟维司群治疗既往接受内分泌治疗后疾病进展的HR阳性、HER2阴性晚期乳腺癌患者的多中心、开放标签、1b期临床试验。嘉和生物的这款产品于2020年6月从G1 Therapeutics公司License-in。
2月,同样来自G1 Therapeutics公司的CDK4/6抑制剂Trilaciclib获FDA审批上市,用于预防扩散期小细胞肺癌成人患者因铂类/依托泊苷方案或拓扑替康方案化学治疗导致的骨髓抑制,同时也是全球唯一一款可降低化疗诱导的骨髓抑制发生率的骨髓保护疗法。
2020年8月,先声药业以高达1.7亿美元从G1 Therapeutics引进Trilaciclib,获得了该产品在大中华地区所有适应症的开发和商业化权益,并于今年4月分别提交了两项临床试验,包括针对转移性结直肠癌患者和小细胞肺癌患者中的III期双盲临床研究。
可以说,CDK4/6抑制剂在国内的研发成功处于爆发的前夕。
雨后春笋般的布局
细胞周期蛋白依赖性激酶(cyclin dependent kinases,CDKs)在细胞周期的启动和各个时期的转换调节中发挥重要作用。CDK4/6与细胞周期蛋白D(cyclin D),可磷酸化视网膜母细胞瘤基因(Rb)继而释放转录因子E2F,促进细胞周期相关基因的转录,使细胞进入S期,CDK4/6抑制剂有效地阻滞肿瘤细胞从G1期进展到S期。特别是在雌激素受体阳性(ER+)乳腺癌中,CDK4/6的过度活跃非常频繁。正因如此,针对某些特性的乳腺癌,CDK4/6抑制剂最受关注。
Tim Hunt、Paul Nurse和Leland H.Hartwell也因上述发现获得了2001年的诺贝尔生理学/医学奖。
目前,全球共批准四款CDK4/6抑制剂上市销售,分别为Palbociclib(Ibrance,哌柏西利)、Ribociclib(Kisqali,利柏西利)、Abemaciclib(Verzenio,阿贝西利)及Trilaciclib(Cosela),2020年全球市场规模为69.92亿美元。
哌柏西利
哌柏西利由辉瑞研发,2015年2月获FDA批准上市,是全球首个用于HR+/HER2-的局部晚期或转移性乳腺癌的CDK4/6抑制剂,与芳香化酶联合使用作为绝经后女性患者的初始内分泌治疗。
自2015年上市以来,哌柏西利就成为治疗乳腺癌的重磅药物,也同时成了辉瑞的摇钱树,2018年销售额为41.18亿美元,2019年49.61亿美元。2020年达53.92亿美元的营收业绩,占据整个CDK4/6抑制剂市场的77%,几乎贡献了辉瑞肿瘤营收的一半。
哌柏西利于2018年7月在中国获批上市,历经两年医保谈判均失败。今年1月,辉瑞宣布将对哌柏西利执行新的价格,每瓶售价从29799元降至13667元,降价幅度达到54%。目前21粒/瓶售价为9244元(75mg)、11521元(100mg)、13667元(125mg)。
阿贝西利
阿贝西利由礼来研发,2017年9月获FDA批准上市,是全球第3款上市的CDK4/6抑制剂,主要用于ER+/HER2-晚期或转移性乳腺癌。
2020年12月,阿贝西利获国家药监局批准,适应症为与芳香化酶抑制剂联用治疗HR+/HER2-女性乳腺癌患者初始内分泌治疗,或与氟维司群联用治疗晚期或转移性HR+/HER2-女性乳腺癌患者。
自上市后阿贝西利销售额逐年攀升,2019年达到5.8亿美元,2020年达到9.13亿美元,增长57%,成为礼来业绩增长的主要驱动药物之一。随着2020年底中国市场的打开,阿贝西利将争夺哌柏西利在中国的市场份额。
利柏西利与Trilaciclib相关情况在上文已提到,不再赘述。
CDK4/6作为明星靶点,在国内俨然已成为一条拥挤的赛道。光是仿制药就有20余家企业布局。齐鲁制药4类仿制药哌柏西利胶囊于2020年12月获批上市,拿下了国内首仿;其余包括科伦、奥赛康、豪森、先声和山香药业5家已经递交上市申请,另有正大天晴等4家企业已开展生物等效性试验,还有11家企业获批临床。
作为创新药研发的项目也是如雨后春笋般冒出,除了上文提到的恒瑞医药外,还有10余家药企已经布局,包括倍而达药业、奥鸿药业、正大天晴等。
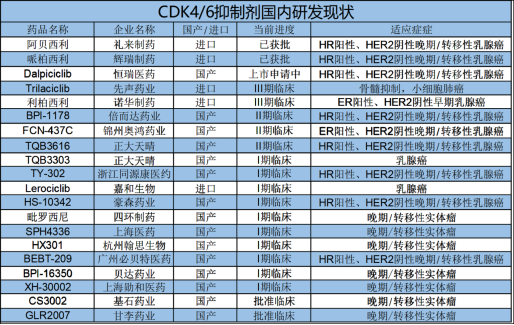
贝壳社整理
结语
在当前创新药发展还处于初期阶段时,往往热门靶点会出现一拥而上的局面。出现这种局面有利有弊,利在于患者能够有更多的选择,弊在于浪费宝贵的临床资源。这是整个创新药行业还不够成熟的表现,相信未来随着政策的约束调整,创新药相关研发将趋于理性。后续发展如何,贝壳社还将持续关注。
参考资料
1、各大上市公司公告、官网
2、《三大CDK4/6抑制剂国内仿制药已获批新药还香吗?》,Insight数据库,2021年6月28日
3、《甘李药业差异化CDK4/6抑制剂国内启动临床》,Insight数据库,2021年10月19日
4、《诺华CDK4/6抑制剂「利柏西利」在华申报上市》,医药魔方,2021年10月22日
5、《嘉和生物GB491启动III期临床,国内CDK4/6抑制剂混战或将开启》,药渡经纬,2021年8月14日
6、《抗癌家族:CDK4/6抑制剂》,药智新闻,2017年6月29日
7、《乳腺癌首次超过肺癌,成为全球新确诊人数最多的癌症》,TOMO放疗中心,2020年12月22日
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..