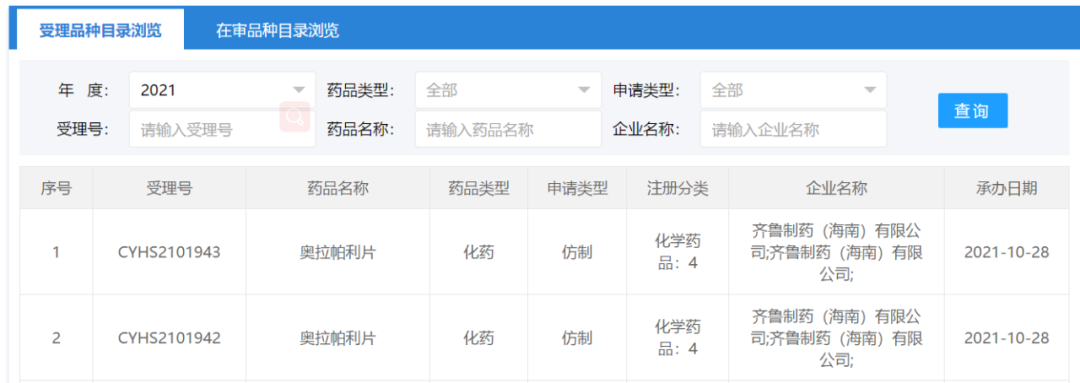
近日CDE官网显示,齐鲁制药按4类申报的奥拉帕利仿制药上市申请获国家药监局受理。这是该产品首个仿制药的上市申请,也是国内首个PARP抑制剂仿制药的上市申请。
奥拉帕利原研为阿斯利康的Lynparza,2014年获FDA批准,是全球首款上市的PARP抑制剂,最初用于BRCA突变的晚期卵巢癌患者,此后其适应症逐渐拓展至胰腺癌、乳腺癌、前列腺癌等的治疗。
2018年8月,奥拉帕利在中国上市(商品名:利普卓),成为国内首个上市的PARP抑制剂和首个卵巢癌靶向新药,目前在国内的适应症具体包括:①铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。②BRCA突变晚期卵巢癌的一线维持治疗。③携带BRCA突变的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌的维持治疗。④单药用于治疗携带胚系或体细胞BRCA突变(gBRCAm或sBRCAm)且既往治疗(包括一种新型内分泌药物)失败的转移性去势抵抗性前列腺癌成人患者。
2019 年,奥拉帕利降价61.8%进入医保乙类目录,2020再降价39.64%,最新医保支付价格为102元/150mg/片。
奥拉帕利自获批以来销售额持续猛增,2020年全球销售额为22.36亿美元,2021上半年达到11.31亿美元,同比增长39%。在中国市场,奥拉帕利持续快速放量,药融云数据显示其2020年全国医院销售额暴涨近23倍达到6亿元,今年上半年销售额已接近去年总额,同比增长183%。
目前国内除了齐鲁制药,豪森药业、正大天晴、山东罗欣等多家药企业也在布局,其中四川科伦、宣泰医药开展并公示了其奥拉帕利片的BE试验。
此外值得一提的是,当前全球共有6款PARP抑制剂上市,分别是奥拉帕利(阿斯利康/默沙东)、尼拉帕利(GSK/再鼎)、氟唑帕利(恒瑞)、帕米帕利(百济神州)、卢卡帕利(Clovis)、talazoparib (辉瑞),其中前4款已在国内获批上市。
文 | 医谷
四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..关于举办2026年度四川省药品生产企业质
各药品生产企业: 2026年是我国..